��Ŀ����
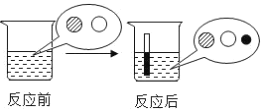
����Ŀ����1����Һ�����ǻ�ѧʵ���ҵij���������Ҫ��50g��������98%��Ũ���ᣬϡ��Ϊ��������20%�����ᣬ����Ҫ��ˮ�����_____mL��ˮ���ܶ�Ϊ1g/cm3��,��ϡ����������ۺ�����ͭ�Ļ�Ϸ�ĩ�У��ȣ���ַ�Ӧ����ˣ�����Һ�м���ྻ��Ƭ����������Һ�е�������_____���ѧʽ������д��������Ӧ�е�һ����ѧ����ʽ_____
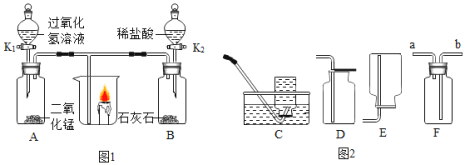
��2�����Na2CO3���г������������Ȼ��ƣ���ѧʵ��С��ͬѧ��ȡ12g������Ʒ�����ձ��У�����ˮʹ����ȫ�ܽ⣬�����еμ��Ȼ�����Һ����������ü����Ȼ������������ɳ���������ͼ��ʾ��
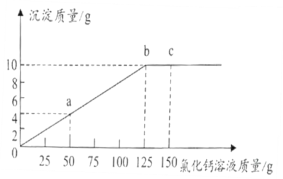
�ټ�����Ʒ��̼���Ƶ���������_____��Ҫ��д��������̣���ȷ��0.1%����
����Ҫ�����Ȼ�����Һ�е������������������������ͼ�е�a��b��c�������ݣ����в��������������_____�����ţ�����Ӧ�����ݡ�
���𰸡�195 FeSO4 CuO+H2SO4==CuSO4+H2O��Fe+CuSO4==FeSO4+Cu 88.3% c
��������
��1������Ҫ��ˮ������Ϊx��50g��98%=20%����50g+x������x=195g������ˮ�����Ϊ��195g��1 g/cm3=195mL��
��ϡ����������ۺ�����ͭ�Ļ�Ϸ�ĩ�У��ȣ���ַ�Ӧ����ˣ�����Һ�м���ྻ��Ƭ������˵��ϡ���ᱻ��ȫ��Ӧ������Һ�е�������FeSO4����д��������Ӧ�е�һ����ѧ����ʽCuO+H2SO4==CuSO4+H2O��Fe+CuSO4==FeSO4+Cu��
��2����Ʒ��̼���Ƶ�����Ϊx
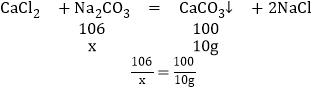
x=10.6g
����Ʒ��̼���Ƶ���������Ϊ��![]()
��c�����Ȼ��ƵĹ�����������Ϊ�����Ȼ����������������ݣ���ѡc��

 ���Ͱ�ͨ��ĩ���ϵ�д�
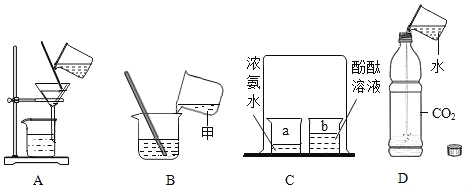
���Ͱ�ͨ��ĩ���ϵ�д�����Ŀ��ѧϰ��ѧҪ��ʵ�����֣�����ʵ�������ȷ���ܴﵽʵ��Ŀ�ĵ���
|
|
|
|
A.Ũ����ϡ�� | B.��ʪ���CO2ͨ����ͼ����װ�� | C.����10.05g���� | D.̽��CO2���ܶȱȿ����� |
A. AB. BC. CD. D