��Ŀ����
�������ȣ�ClO2������������ˮ�������Դ���Ϊԭ������ClO2�Ĺ�����Ҫ������
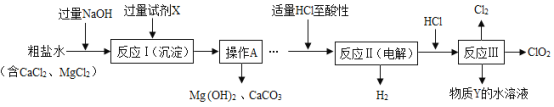
�ٴ��ξ��ƣ������������µ��NaCl��Һ��NaClO3����ClO2����ȡ������������ͼ�����з�Ӧ����ȡClO2�Ļ�ѧ����ʽΪ2NaClO3+4HCl=2ClO2��+Cl2��+2NaCl+2H2O�����ڸ�ʵ�������˵������ȷ����
A.������X��̼������Һ������Y��ѭ������
B.����A�������ǹ��ˣ��õ��IJ��������в�������©�����ձ�
C.��Ӧ��Ļ�ѧ����ʽΪ��2H2O 2H2��+ O2 ��
2H2��+ O2 ��
D.Ϊ��߾���Ч�棬���������пɽ�H2��Cl2�Ƴ�HCl�������
�±��г���һЩ���������ڳ����µ�pH��Χ�����гʼ��Ե���
�������� | ������ | ţ�� | ������ | ƻ��֭ |
pH��Χ | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.9~3.3 |
A.������
B.ţ��
C.������
D.ƻ��֭
��ȤС���ͬѧ��̼�����ơ�̼���ơ��������Ƶ�ijЩ���ʽ������̽����
��������⣩������Һ������Լ����ᷴӦʱ��Һ��pH��α仯��
��ʵ��̽��1������������Ũ�ȵ�̼�����ơ�̼���ơ�����������Һ�У��ֱ���뼸���ϸ���֭Һ��ͬʱ������ˮ���жԱ�ʵ�飬�۲첢��¼�������£�
Һ������ | ����ˮ | ̼��������Һ | ̼������Һ | ����������Һ |
�ϸ���֭Һ��ʾ����ɫ | ����ɫ | ��ɫ | ��ɫ | ��ɫ |
�������ϣ�
pH | 7.5��9 | 10��11.9 | 12��14 |
�ϸ���֭Һ��ʾ����ɫ | ��ɫ | ��ɫ | ��ɫ |
���ó�����1��������Һ�ļ�����ǿ������˳��Ϊ______��
��ʵ��̽��2����ͬѧ���ձ���Һ�м���Լ5mLϡ����������Һ�����뼸�η�̪��Һ����ʱ��Һ����ɫ��Ϊ_____ɫ�������м���ϡ���ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ______����ͬѧ��һ�������һ��Ũ�ȵ�����������Һ�У���μ���һ��Ũ�ȵ����ᣬ�õ�pH�仯��ʱ��Ĺ�ϵ��ͼ1��ʾ.

���ó�����2�����۽Ƕȷ������÷�Ӧ��ʵ����___________��
��ʵ��̽��3��������������̼ԭ������̼�����ƺ�̼������Һ�У��ֱ���μ���һ��Ũ�ȵ����ᣬ�õ�pH�仯��ʱ��Ĺ�ϵ��ͼ2��ͼ3��ʾ��
�������뷴˼��b�������Ϊ______��д��ѧʽ������ͼ2��ͼ3����Ӱ���ֽ��е��ӣ������������غϡ�
���ó�����3��ͨ������������̼���ƺ����ᷴӦ���̣���������������������ѧ����ʽ��ʾ��Na2CO3+HCl=NaCl+NaHCO3��_____________��
�������뷴˼��̽����Һ������Լ���ӦpHֵ�ı仯��������ʶ��Ӧ��ԭ�������еĹ��̡�


