题目内容
【题目】根据下列实验装置图,按要求回答下列问题:
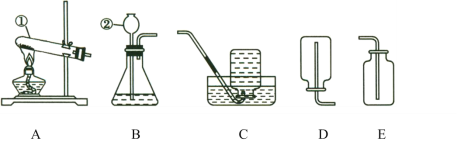
(1)写出标有序号的仪器名称:______________;______________。
(2)实验室制取CO2的化学反应方程式为_______________________________________;制取并收集该气体应选择的装置是______________(填序号);写出选用仪器②的优点是______________;检验该气体的方法是_____________________________。
(3)如果选择与制取CO2相同的发生装置来制取O2,则发生反应的化学方程式为___________,其基本反应类型是______________。
【答案】试管 长颈漏斗 CaCO3+2HCl=CaCl2+H2O+CO2↑ BE 可以控制反应速率 将气体通入澄清的石灰水,观察是否变浑浊 2H2O2![]() 2H2O+O2↑ 分解反应
2H2O+O2↑ 分解反应
【解析】
(1)写出标有序号的仪器名称:①试管②长颈漏斗;
(2)实验室用稀盐酸和大理石制取CO2的化学反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;制取二氧化碳气体选择固液发生装置B,收集该气体应选择向上排空气法收集,选择装置E;仪器②的优点是:可以控制反应速率;检验该气体的方法是:将气体通入澄清的石灰水,观察是否变浑浊;
(3)如果选择与制取CO2相同的固液发生装置来制取O2,则双氧水在二氧化锰催化剂作用下发生反应的化学方程式为:2H2O2![]() 2H2O+O2↑,该反应符合“一变多”,属于分解反应。
2H2O+O2↑,该反应符合“一变多”,属于分解反应。

 阅读快车系列答案
阅读快车系列答案【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。