题目内容
【题目】2018年10月24日,港珠澳大桥正式开通,让世人再次见证我国在基础设施建设方面的巨大成就。大桥建设过程使用了大量的石灰石资源。

(1)煅烧石灰石可制得CaO,为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图1所示。
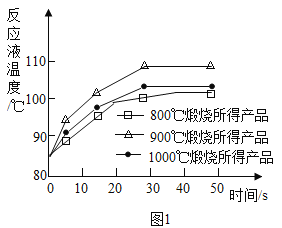
可知:CaO与H2O反应会热量_____(填“放出”或“吸收”);上述温度中,_____℃烧所得CaO活性最高。要得出正确结论,煅烧时还需控制的条件是_____。
(2)以电石渣[主要成分为Ca(OH)2,还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如图2:
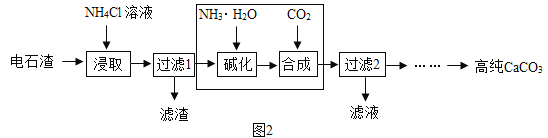
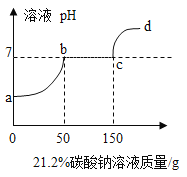
图3为NH4Cl浓度对钙、镁浸出率的影响
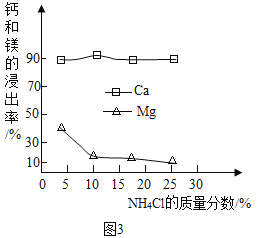
(浸出率=![]() ×100%)
×100%)
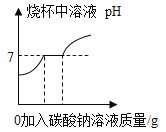
可知:①较适宜的NH4Cl溶液的质量分数为_____;浸取时主要反应的化学方程式为_____,反应类型属于_____。
②流程中线框内部分若改用_____溶液(填化学式),也可一步得到与原流程完全相同的生成物。
【答案】放出 900 煅烧时间相同 10% ![]() 复分解反应 NH4HCO3或Na2CO3(合理即可)
复分解反应 NH4HCO3或Na2CO3(合理即可)
【解析】
(1)氧化钙和水反应生成氢氧化钙,放出热量,通过分析表中的数据可知,900℃时所得CaO活性最高,要得出正确结论,煅烧时还需控制的条件是煅烧时的时间;
(2)①通过分析图象中氯化铵浸出钙离子的质量分数可知,较适宜的NH4Cl溶液的质量分数为10%,氯化铵和氢氧化钙反应生成氯化钙、氨气和水,所以浸取时主要反应的化学方程式为:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O,该反应属于复分解反应;
②图中的流程分析可知,碳酸氢铵和氨水、二氧化碳所起的作用是相同的,所以流程中虚线内部分若改用NH4HCO3溶液。
故答案为:(1)放出;900;煅烧时的时间;
(2)①10%;2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O;复分解反应;②NH4HCO3。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】胃舒平(含Al(OH)3)、小苏打片(含NaHCO3)、胃酸抑制剂(主要含CaCO3、Mg(OH)2)都是常用的中和胃酸的药物。
(1)胃舒平与胃酸发生反应的化学方程式为:_____。
(2)为了探究工业小苏打中是否含少量的NaCl,设计如下实验:(假设小苏打片中其他物质均不含Cl-)
实验步骤 | 实验现象 | 实验结论 |
第一步:取1片小苏打于试管中,加入适量水充分溶解,再滴加足量的稀HNO3。 | 有_____产生 | 说明小苏打片中含有NaHCO3。 |
第二步:再往上述溶液中滴加少量_____溶液。(写化学式) | 有_____产生 | 说明小苏打片中含有NaCl。 |
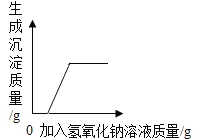
(3)胃酸抑制剂每片lg,取10片于烧杯中,再加入50g稀HCl,烧杯中剩余物的质量与时间的关系如下表:(已知其他物质不与稀盐酸反应)
时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
剩余物的质量/g | 60 | 59.12 | 58.24 | 57.36 | 56.48 | 56.48 |
求每片胃酸抑制剂中CaCO3的质量分数_____(写出计算过程)。