题目内容
【题目】(8分)某同学在做实验时得知氯化钠样品中含有少量泥沙、氯化钙和氯化镁,于是设计了以下流程除去氯化钠样品中泥沙、氯化钙和氯化镁。
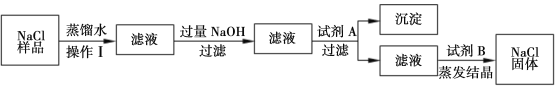
请根据流程图回答:
(1)操作Ⅰ的名称是 ,试剂A是 ,试剂B是 。
(2)写出NaOH与杂质反应的化学方程式 。
(3)蒸发结晶时玻璃棒的作用是 。
(4)用提纯后的氯化钠固体来配制50g质量分数为6%的氯化钠溶液,其步骤为:①计算、②称量、③ 、④ 溶解、⑤装入试剂瓶中,盖好瓶塞并 。
【答案】(1)过滤;Na2CO3 ; HCl(2)2NaOH+MgCl2=Mg(OH)2↓+2NaCl(3)搅拌,防止因局部温度过高,造成液滴飞溅(4)量取 贴上标签
【解析】
试题分析:(1)因为操作一后,固液分离,故操作Ⅰ的名称是 过滤;试剂A为除去钙离子的碳酸钠溶液;试剂B是除去过量的氢氧化钠和碳酸钠的鉴别稀盐酸;(2)NaOH与杂质氯化镁反应的化学方程式为2NaOH+MgCl2=Mg(OH)2↓+2NaCl,(3)蒸发结晶时玻璃棒的作用是搅拌,防止因局部温度过高,造成液滴飞溅;(4)用提纯后的氯化钠固体来配制50g质量分数为6%的氯化钠溶液,其步骤为:①计算、②称量、③量取,④ 溶解、⑤装入试剂瓶中,盖好瓶塞贴上标签。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目