题目内容
【题目】汽车尾气三效催化剂表面物质转化的关系如右下图所示,下列说法错误的是 ( )
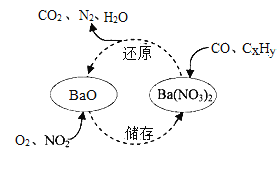
A.储存过程发生了化合反应
B.该过程能减缓温室效应和酸雨污染
C.还原过程中CxHy生成的CO2和H2O质量比为22 : 9,则x: y=1:2
D.整个转化过程中有机物除外的化学方程式可表示为: 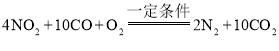
【答案】C
【解析】
A、储存过程是氧气和二氧化氮以及氧化钡反应生成硝酸钡,符合化合反应“多变一”特征,属于化合反应,正确;
B、过程消耗了二氧化氮和碳氢化合物,所以能减缓温室效应和酸雨污染,正确;
C、还原过程生成CO2和H2O质量比为22:9,可得碳原子和氢原子个数比为![]() :(
:(![]() )=1:2,但由于过程中有一氧化碳反应,所以不能确定x:y=1:2,错误;
)=1:2,但由于过程中有一氧化碳反应,所以不能确定x:y=1:2,错误;
D、整个转化反应(有机物除外)的总化学方程式可表示为:4NO2+10CO+O2 2N2+10CO2,正确;
2N2+10CO2,正确;
故选:C。

 名校课堂系列答案
名校课堂系列答案【题目】实验课上,某小组的同学用块状生石灰进行“化学反应中能量的变化”实验时发现:向块状生石灰样品中加入适量水后没有明显的温度变化。为确定其原因,进行了如下实验探究。实验验证一。
[提出问题]生石灰是否变质?其成分是什么?
[查阅资料]氢氧化钙溶解过程中无明显温度变化,与盐酸反应无气体生成。
[猜想与假设]同学们认为块状生石灰样品已变质,并对其成分作出了如下4种猜想。
猜想1:氧化钙和氢氧化钙:猜想2:氧化钙和碳酸钙:猜想3:______________;
猜想4:氧化钙、氢氧化钙和碳酸钙。
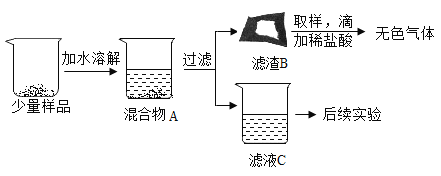
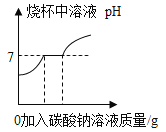
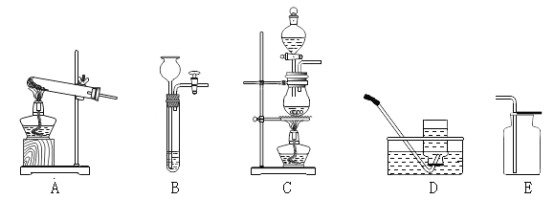
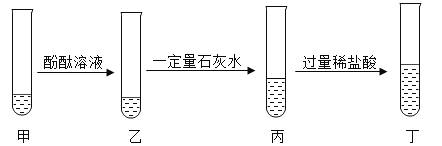
[进行实验]同学们将少量样品研碎后,按如图所示过程进行实验。
(1)在溶解过程中用温度计测量液体的温度,发现温度计示数升高,说明样品中应该含有______________。
[结论]猜想3不成立。
(2)滤渣B中一定含有_____________,用化学方程式表示变质过程中生成该物质的反应_____________。
[结论]①块状生石灰表面发生变质:②猜想1不成立。
(3)为验证滤液C的成分,进行后续实验。
实验操作 | 实验现象 | 实验结论 |
____________ | ____________ | ② 滤液中溶质为氢氧化钙 ②猜想4成立,猜想2不成立 |
[反思与评价]
(4)有的同学认为上述实验过程不能得出猜想4成立、猜想2不成立的结论,理由是______________。
[注意:答对15题以下小题奖励4分,化学试卷总不超过60分]
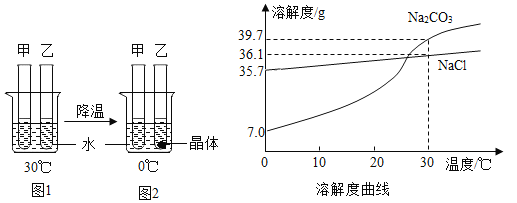
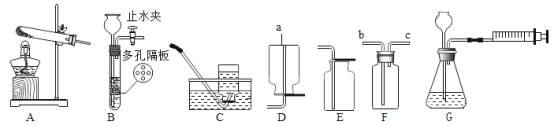
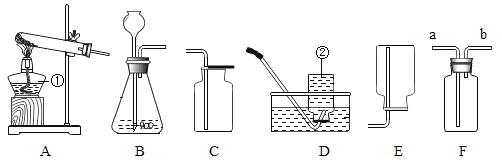
实验验证二:为了进一步确定块状生石灰样品的成分及质量,实验小组利用如下图所示的装置(夹持仪器省略)进行实验。
查阅资料:氢氧化钙加热至580°C、碳酸钙加热至825°C分别分解生成两种氧化物。
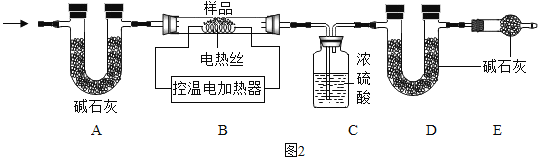
(5)①装置E的作用是______________。
②控温电加热器使装置B中反应完全,再通一段时间空气,测得反应前后装置C、D分别增重18.0g和22.0g,将装置B中反应后剩余的固体氧化物加入足量水中溶解,蒸发所得固体(不含水)增重36. 0g.求原块状生石灰固体样品中各成分为______________,各物质的质量______________。
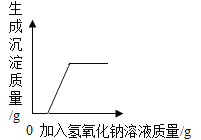
【题目】实验技能训练中,小亮同学向氧化铜和稀硫酸充分反应后的废液中加入一定量的氢氧化钠溶液,发现无明显现象。小亮同学在老师的指导下对反应后的废液进行了实验:他分别取50g废液,并向其中逐渐加入等浓度的氢氧化钠溶液,三组实验的数据与其中一组的图象如下:
实验组数 | 第一组 | 第二组 | 第三组 |
加入氢氧化钠溶液质量/g | 50 | 100 | 80 |
产生沉淀的质量/g | 0.98 | 2.94 | 2.94 |
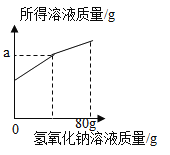
请根据以上信息回答下列问题:所得
(1)废液中的溶质有_____(填化学式)。
(2)计算废液中硫酸铜的溶质质量分数。_____(写出计算过程)
(3)若三组数据中,只有某一组加入的氢氧化钠溶液与废液恰好完全反应,则该实验为第_____组,下图中a的数值为_____。