题目内容
【题目】下列装置是实验室常用气体制备装置,据图回答问题:
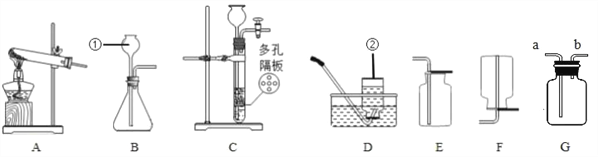
(1)写出编号为①、②的仪器名称_______________、_______________
(2)实验室制备气体时,应对装置先______________ ,选用 A 装置做制取氧气的发生装置,发 生反应的化学方程式为_____________________________ 。若选用装置 E 的方法收集氧气,则判断氧气 已收集满的方法是_____________________________ 。
(3)实验室用过氧化氢溶液和二氧化锰制备较纯净的氧气时,应选的收集装置为_____(填字母),发生反应的化学方程式是_________。该实验不能选择 C 装置作为发生装置的原因是_____。二氧化锰在该反应中起_____而使得反应很剧烈,据此提出实验安全注意事项或改进措施是______________。(请 填写序号)
①改用能控制滴液速度的仪器; ②用小体积的锥形瓶;
③加热反应物; ④降低反应物浓度
(4)实验室制取氢气的化学反应原理是_____,若选用 C 作为氢气的发生装置其优点是 ______。当 G 装置中盛满水,氢气从 _____(填“a”或“b”)端导入,另外一端再加配________(填一种仪器名称)就 可以达到收集并测量氢气体积的目的。
(5) 在实验室里可用硫化亚铁固体和稀硫酸的反应来制取硫化氢气体,同时还生成了一 种在溶液中呈浅绿色的硫酸盐。该反应的化学方程式为________________。在 通常情况下硫化氢是一种无色、有臭鸡蛋气味的有毒气体,密度比空气大且能溶于水。实 验室制取硫化氢应选择_____(填字母)作为收集装置,并在通风橱中进行操作,还要 有尾气处理装置。
【答案】 长颈漏斗 集气瓶 检查气密性 略 将带火星的木条放在集气瓶口,若木条复燃,则已满 D 略 MnO2 是粉末状固体易从隔板漏下 催化作用 ①④ 略 可控制反应的发生和停止 b 量筒 略 E 或 G
【解析】【试题分析】本题考查了初中化学气体的制备。一般常考查气体发生装置、收集装置选择。学习中应注意实验仪器的识别、用途及选择装置的依据的总结。
(1)①、②的仪器名称分别是长颈漏斗、集气瓶;
(2)制备气体时,在连接好装置后,首先进行气密性的检查,选用 A 装置做制取氧气,根据反应物的状态、反应的条件和试管口没有放一团棉花应选择氯酸钾和二氧化锰的混合物加热制取氧气,故反应的化学方程式为:2KClO3![]() 2KCl+3O2↑, 选用装置 E 的方法收集氧气,判断氧气 已收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则已满,
2KCl+3O2↑, 选用装置 E 的方法收集氧气,判断氧气 已收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则已满,
(3)排水法收集到的气体比排空气法收集到的气体纯净,故制备较纯净的氧气时,应选的收集装置为排水法,故选D;装置C是利用隔板能将反应物中块状固体和液体分开,达到控制反应的发生和停止, MnO2 是粉末状固体易从隔板漏下,故不能选择 C 装置作为发生装置;二氧化锰在该反应中起催化作用而使得反应很剧烈;
①改用能控制滴液 速度的仪器,可控制液体与固体的接触,达到控制反应速率的目的,故正确,
②发生装置中反应剧烈,产生气体速率快,用体积小的锥形瓶会引起爆炸,故错误,
③加热反应物会使反应速率加快,导致反应更加剧烈,产生危险,故错误,
④降低反应物浓度,会导致反应速率降低,故正确。
(4)实验室制取氢气的化学反应原理是Zn+H2SO4=ZnSO4+H2↑,选用 C 作为氢气的发生装置其优点是可控制反应的发生和停止,用盛满水的G装置收集氢气,氢气密度比水小,应从b进入,测量所得气体的体积需增加量筒. 硫化氢密度比空气大且能溶于水,所以不能用排水法收集,应用向上排空气法收集,故应选用E 或 G。
(5) 硫化亚铁固体和稀硫酸的反应来制取硫化氢气体化学方程式为FeS+H2SO4=FeSO4+H2S,

【题目】下图是某燃气热水器的内部构造示意图。
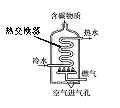
⑴ 若该热水器采用天然气为燃气。
① 当“空气进气孔”堵塞,该热水器有黑色物质附着,原因:________(用化学方程式解释)
② 燃料不完全燃烧时还可能会生成_______造成人体中毒;
③ 燃气热水器中的热交换器采用了回形管结构,它的优点是_________。
⑵ 热值是指1kg某种燃料完全燃烧放出的热量,常见三种燃料的热值及1kg燃料燃烧产生的CO2和SO2的质量如下表。
燃料 | 热值kJ/kg | 燃烧产物的质量/g | |
二氧化碳 | 二氧化硫 | ||
汽油 | 约48000 | 2900 | 5.0 |
天然气 | 约56000 | 2500 | 0.1 |
煤 | 约33000 | 2500 | 11.0 |
结合上表数据分析:以上三种燃料中最清洁高效的能源是______,理由是______。