题目内容
【题目】20℃时,将不同质量的NaCl晶体分别加入100g水中,充分溶解后所得溶液质量与加入NaCl晶体质量的对应关系如表:
组别 | A | B | C | D | E |
NaCl晶体质量/g | 5 | 15 | 20 | 30 | 40 |
所得溶液质量/g | 105 | 115 | X | 130 | 136 |
请回答下列问题:
(1)A组的溶液为(填“饱和”或“不饱和”)溶液.
(2)C组X的值为 .
(3)如图为NaCl的溶解度曲线图,图上a点纵坐标的值为 . Ca(OH)2的溶解度温度变化的趋势与NaCl相反,则室温时,向饱和石灰水加入少量生石灰,并恢复到室温,此时溶液中溶质的质量(填“>”、“<”或“=”)原溶液中溶质的质量. 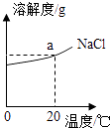
【答案】
(1)不饱和
(2)120
(3)36;<
【解析】解:(1)根据题意可知A组中还能继续溶解氯化钠固体,所以为不饱和溶液;故填:不饱和;(2)氯化钠的溶解度随温度的升高而增大,20℃时100g水中能溶解20g氯化钠,所以C组X的值为100+20=120;故填:120;(3)根据题意可知,20℃时100g水中最多溶解36g氯化钠,所以图上a点纵坐标的值为36,氧化钙和水反应生成氢氧化钙,向饱和石灰水加入少量生石灰,水的质量减少,并恢复到室温,此时溶液还是该温度的饱和溶液,所以所得溶液中溶质的质量小于原溶液中溶质的质量.故填:<.
【考点精析】本题主要考查了饱和溶液和不饱和溶液和固体溶解度曲线及其作用的相关知识点,需要掌握饱和与不饱和的判断方法:看有无不溶物或继续加入该溶质,看能否溶解;1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和)才能正确解答此题.

【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
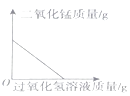
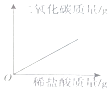
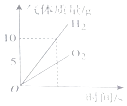
A.向一定量的二氧化锰中加入过氧化氢溶液 | B.向一定量的水中加入少量氯化钠 | C.向一定量石灰石中滴加稀盐酸 | D.将水通电电解一段时间 |
A.A
B.B
C.C
D.D