题目内容
【题目】科学兴趣小组学习了二氧化锰(MnO2)催化分解过氧化氢的实验后,进行如下实验.
(一)选择装置并检查气密性.
(二)称取0.1克的二氧化锰粉末加入容器中.
(三)量取50毫升溶质质量分数约10%的过氧化氢溶液加入容器中,记录一定时间内收集到的气体体积.
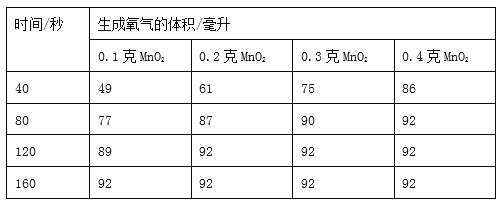
(四)改变二氧化锰的质量,重复上述实验,记录数据如下.
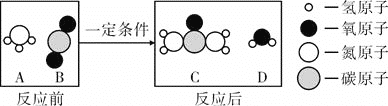
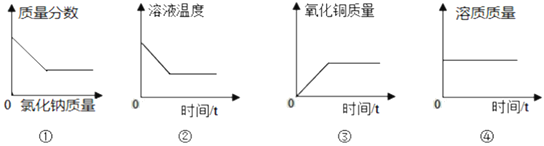
(1)写出本实验的化学方程式____.随着反应的进行,溶液中____(填写化学式)在不断地减少、溶剂在不断地____(填增多、减少、不变).
(2)本实验探究的问题是____.
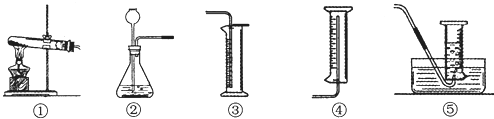
(3)实验中除了量筒外,还需要用到的测量仪器有____.
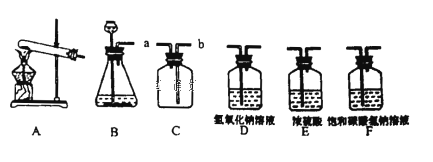
(4)为完成本实验,应选择右上图图气体发生和收集装置中的组合是____(选填序号).你选择的气体发生装置的理由是____.
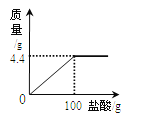
(5)在40秒时,通过四组数据分析,你得出的结论是____.
(6)若实验前加入MnO20.1g,实验后经过滤、洗涤、干燥、称量,MnO2质量为____g.请设计实验证明该MnO2的化学性质在反应前后没有改变____.
【答案】2H2O2![]() 2H2O+O2↑H2O2增多二氧化锰的质量对过氧化氢分解快慢的影响天平、停表(或秒表)②⑤反应物的状态(固体和液体)且不加热在该时间内,MnO2的质量愈多,H2O2分解速率愈大(MnO2催化效果愈好)0.1取少量相同质量的氯酸钾于试管中,并向其中的一支试管中加入上述MnO2拌和。同时加热两支试管并在试管的上方各放带火星(燃着)的木棒,若盛放MnO2的试管上方的木棒先复燃(燃烧的更旺),则可证明MnO2的化学性质不变
2H2O+O2↑H2O2增多二氧化锰的质量对过氧化氢分解快慢的影响天平、停表(或秒表)②⑤反应物的状态(固体和液体)且不加热在该时间内,MnO2的质量愈多,H2O2分解速率愈大(MnO2催化效果愈好)0.1取少量相同质量的氯酸钾于试管中,并向其中的一支试管中加入上述MnO2拌和。同时加热两支试管并在试管的上方各放带火星(燃着)的木棒,若盛放MnO2的试管上方的木棒先复燃(燃烧的更旺),则可证明MnO2的化学性质不变
【解析】
(1)根据反应方程式的书写方法和反应中反应物在减少,生成物在增加考虑;
(2)根据(二)、(三)所用物质和(四)中提供的数据进行推测;
(3)根据实验中要称取二氧化锰,并要计时分析所需测量仪器;
(4)根据过氧化氢溶液和二氧化锰反应是固体和液体的不加热反应选择发生装置;根据氧气的密度和水溶性选择收集装置;
(5)根据在该时间内生成氧气的体积数值比较考虑;
(6)根据催化剂反应前后质量不变考虑,根据催化剂的重复使用性考虑。
(1)反应物是过氧化氢写在等号的左边,生成物是水和氧气写在等号的右边,用观察法配平,所以方程式是:2H2O2![]() 2H2O+O2↑;由于在反应中过氧化氢属于反应物,在不断的消耗,所以质量在不断减少;生成物是水和氧气,所以溶液中的溶剂水在不断增加;
2H2O+O2↑;由于在反应中过氧化氢属于反应物,在不断的消耗,所以质量在不断减少;生成物是水和氧气,所以溶液中的溶剂水在不断增加;
(2)从题干中提供的信息可知,所用过氧化氢溶液的量和质量分数都是相同的,只是三次加入的二氧化锰的量不同,并且记录了在不同量二氧化锰的条件下,不同时间生成的氧气的量。可见此实验探究达到问题是:二氧化锰的质量对过氧化氢分解快慢的影响;
(3)实验中要称取二氧化锰,所以要用到天平;并要计时,所以用秒表;
(4)过氧化氢溶液和二氧化锰反应是固体和液体的不加热反应,可用装置②完成;氧气密度大于空气密度,并且不易溶于水,所以可用向上排空气法和排水法收集,要记录一定时间内收集到的气体体积,所以用②⑤合适;
(5)在40秒时,通过观察在该时间内生成氧气的体积数值比较可知,MnO2的质量愈多,H2O2分解速率愈大;
(6)催化剂反应前后质量不变,所以实验后经过滤、洗涤、干燥、称量,MnO2质量仍然为0.1g;从过氧化氢分解后的混合物中回收二氧化锰,再将其放在氯酸钾中加热,利用带火星的木条检验生成氧气的快慢。所以取少量相同质量的氯酸钾于试管中,并向其中的一支试管中加入上述MnO2拌和。同时加热两支试管并在试管的上方各放带火星(燃着)的木棒,若盛放MnO2的试管上方的木棒先复燃(燃烧的更旺),则可证明MnO2的化学性质不变。

【题目】今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
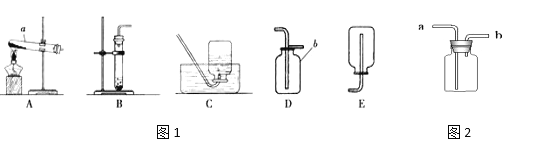
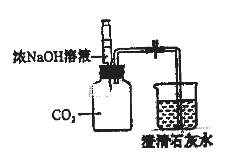
(1)写出图3中标有序号的仪器名称a_______
(2)①此气体是什么物质?验证它的实验方案如下:
猜想 | 实验步骤 | 现象及结论 |
此气体可能是:_____ | ______________ | ______________ |
②产生此气体的化学方程式可能是_________;
③我想制取该气体,可以分别选取图1中的______作发生装置和________作收集装置(填序号);
④如用图2装置收集该气体,气体由 ________端导入;
⑤若用加热高锰酸钾来制取氧气,所选用的发生装置是________(在图1中选择),产生氧气的化学方程式是:_____________。