题目内容
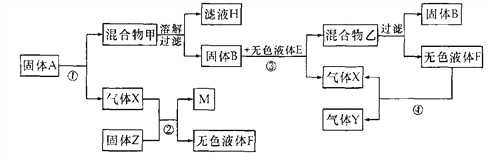
【题目】某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】(1)取部分该干燥剂于试管中,加水无放热现象,说明干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下二种方案。
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中。请你参与实验,并填写表中的空白:
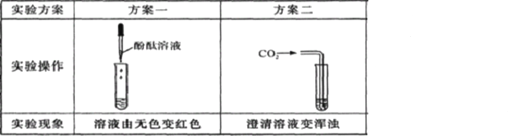
写出方案二发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思生石灰干燥剂变质原因,认识到实验室保存氧化钙应注意 。
【答案】⑴CaO或氧化钙
⑵CaCO3或碳酸钙。 Ca(OH)2+CO2==CaCO3↓+H2O
四 密封保存 (其他合理答案均可)
【解析】分析:首先要仔细阅读题中所给的信息,抓到题干中的相关信息.对于第一小题(1)在该干燥剂中加入书水没有发热现象,根据知识点生石灰与水变熟石灰放出大量热可知一定不含生石灰;第二小题探究(2)中加足量酸有气泡推断肯定含有碳酸盐那么可以判断出该干燥剂中一定含有了碳酸钙;第三小题根据三个方案的实验探究,首先第一个实验方案指示剂的颜色变化肯定含有碱性物质,第二个方案通入二氧化碳变浑浊说明含有氢氧化钙;第三个方案也更说明含有氢氧化钙更由此猜想四是正确的.通过科学实验探究我们应该反思:在化学实验室保存氢氧化钙是一定不能漏置在空气中,否则会与空气中的二氧化碳发生反应而变质.
解答:(1)加水没有发热现象根据氧化钙(生石灰)的特性可以判断一定没有生石灰存在.因此正确答案:CaO或氧化钙;
(2)加入足量的酸有气泡产生说明该干燥剂中一定含有 CaCO3,但不能判断是否一定还有氢氧化钙,因Ca(OH)2遇到酸不会有气泡产生所以不能判定一定含有氢氧化钙.故正确答案:CaCO3或碳酸钙;
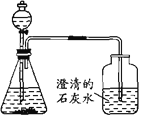
(3)常用澄清的石灰水来检验二氧化碳的存在,它会变浑浊是白色沉淀物碳酸钙,对于沉淀一定要加沉淀号↓;此为是水.所以化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;由以上实验探究得出猜想一,二,三都不可能有这几种情况的存在故答案:四; 由于氢氧化钙会和空气中的二氧化碳发生反应而变质所以要避免与空气接触即正确答案:密封保存

 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.
(1)地壳中含量最高的金属元素是__________.
(2)根据图示金属应用实例推断,金属具有的物理性质有___________________.

(3)日常使用的金属材料多数属于合金.表中列出了一些常见合金的主要成分和性能.
合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃ |
硬铝 | 强度和硬度好 | 铝、铜、镁等.硬度小,质软 |
不锈钢 | 抗腐蚀性好 | 铁、铬、镍等.纯铁抗腐蚀性能不如不锈钢 |
由上表推断,与组成合金的纯金属相比,合金的优点一般有________________.
①强度更低②硬度更高 ③熔点更高 ④抗腐蚀性更好
(4)人们每年要从金属矿物资源中提取数以亿吨计的金属.根据所学化学知识,按要 求写出两个生成金属的化学方程式:
①___________________________________________________(置换反应);
②___________________________________________________(分解反应) .
(5)2008年奥运会主运动场“鸟巢”使用了大量的钢铁.钢铁与_____________直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈.