题目内容
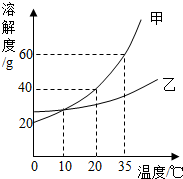 (2013?泉州)如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )
(2013?泉州)如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )分析:A、根据某一温度时物质溶解度的比较方法考虑;B、根据35℃时甲的溶解度进行分析;C、根据降低温度时甲物质的溶解度减小进行分析;D、根据10℃时甲、乙两种的溶解度相等,饱和溶液的溶质质量分数相等考虑.
解答:解:A、比较两种物质溶解度的大小,必须有温度的限制,故A错;
B、35℃时甲的溶解度是60g,即该温度下,100g水中最多溶解60g甲,所以35℃时160g甲的饱和溶液中含甲的质量60g,故B错;
C、降低温度时甲物质的溶解度减小,会析出晶体,所以溶液仍然是饱和溶液,故C正确;
D、10℃时甲、乙两种的溶解度相等,饱和溶液的溶质质量分数相等,没说明溶液是否饱和,不能比较溶质质量分数的大小,故D错.
故选C.
B、35℃时甲的溶解度是60g,即该温度下,100g水中最多溶解60g甲,所以35℃时160g甲的饱和溶液中含甲的质量60g,故B错;
C、降低温度时甲物质的溶解度减小,会析出晶体,所以溶液仍然是饱和溶液,故C正确;
D、10℃时甲、乙两种的溶解度相等,饱和溶液的溶质质量分数相等,没说明溶液是否饱和,不能比较溶质质量分数的大小,故D错.
故选C.
点评:解答本题关键是要知道比较两种物质溶解度的大小,必须有温度的限制,知道溶解度的四要素:一定温度,100g溶剂,饱和状态,溶解的质量;知道不饱和溶液变为饱和溶液的方法.

练习册系列答案
相关题目
 (2013?泉州质检)妈妈为小志的十六岁生日聚会准备了很多物品,其中蕴含着丰富的化学知识,请回答:
(2013?泉州质检)妈妈为小志的十六岁生日聚会准备了很多物品,其中蕴含着丰富的化学知识,请回答: