题目内容
(2013?泉州)如图1所示的仪器和装置,可用于实验室制取氧气,请回答有关问题:
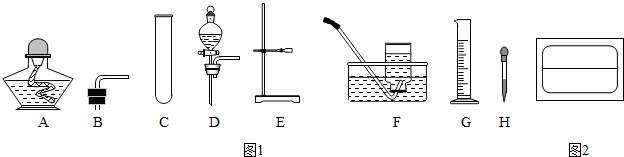
(1)用高锰酸钾制取氧气,该反应的化学方程式是
(2)实验室也可以用双氧水来制取氧气,实验时还需加入少量二氧化锰,其作用是
(3)在量取水的操作中,当水面接近所需刻度时,应改用
(4)用F装置来收集氧气时,若集气瓶口有气泡冒出,说明集气瓶内的氧气已收集满,接下来的操作是

(1)用高锰酸钾制取氧气,该反应的化学方程式是
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
,其气体发生装置可选择上图中的
| ||
ABCE
ABCE
(填标号)组合.从所选的组合中选择某一种仪器,写出它的名称:A,酒精灯(或E,铁架台等)
A,酒精灯(或E,铁架台等)
,简要说出它的用途:用作热源(或用于支持固定等)
用作热源(或用于支持固定等)
.(2)实验室也可以用双氧水来制取氧气,实验时还需加入少量二氧化锰,其作用是
催化作用
催化作用
.现要配制100g溶质质量分数为6%的双氧水溶液,需要30%的双氧水溶液20
20
g,需要加入水的体积为80
80
mL.(3)在量取水的操作中,当水面接近所需刻度时,应改用
H
H
(填标号)加水至所需刻度.将配制好的溶液装入试剂瓶中,贴好标签.请在如图2所示的标签内填入试剂瓶所要贴的标签内容.(4)用F装置来收集氧气时,若集气瓶口有气泡冒出,说明集气瓶内的氧气已收集满,接下来的操作是
在水面下用玻璃片盖住集气瓶口
在水面下用玻璃片盖住集气瓶口
,然后将集气瓶移出水面,正放在桌面上.分析:(1)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,写出反应的化学方程式;根据发生装置的特点选择需要的仪器;
(2)用双氧水来制取氧气,实验时还需加入少量二氧化锰作为催化剂,改变了过氧化氢的分解速率;
根据溶液加水稀释前后溶质的质量不变,依据计算公式:M(浓)×W(浓)=M(稀)×W(稀)进行分析解答;
(3)根据使用量筒的方法回答:先倒后滴的原则,并写上标签:溶质的质量分数和溶液的名称;
(4)根据用排水法收集氧气的注意事项分析.
(2)用双氧水来制取氧气,实验时还需加入少量二氧化锰作为催化剂,改变了过氧化氢的分解速率;
根据溶液加水稀释前后溶质的质量不变,依据计算公式:M(浓)×W(浓)=M(稀)×W(稀)进行分析解答;
(3)根据使用量筒的方法回答:先倒后滴的原则,并写上标签:溶质的质量分数和溶液的名称;
(4)根据用排水法收集氧气的注意事项分析.
解答:解:(1)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;该发生装置的特点是固体加热型,移出需要的仪器有:酒精灯、试管、导气管、铁架台;其中酒精灯的作用是加热,用作热源(或铁架台,用于支持固定等);
(2)用双氧水来制取氧气,实验时还需加入少量二氧化锰,其作用是催化作用;
根据稀释前后过氧化氢的质量前后保持不变,设需要30%的双氧水的质量为x,依据计算公式可得:
100g×6%=30%x,
则 x=20g; 需要水的质量为:100g-20g=80g即80ml;
(3)在量取水的操作中,当水面接近所需刻度时,应改用胶头滴管加水至所需刻度;标签上的内容是:
(4)用排水法收集满氧气后,接下来的操作是在水面下用玻璃片盖住集气瓶口,然后将集气瓶移出水面,正放在桌面上;
故答案为:(1)2KMnO4
K2MnO4+MnO2+O2↑;ABCE;A,酒精灯(或E铁架台等);用作热源(或用于支持固定等);
(2)催化作用;20;80;(3)H;

(4)在水面下用玻璃片盖住集气瓶口.
| ||
(2)用双氧水来制取氧气,实验时还需加入少量二氧化锰,其作用是催化作用;
根据稀释前后过氧化氢的质量前后保持不变,设需要30%的双氧水的质量为x,依据计算公式可得:
100g×6%=30%x,
则 x=20g; 需要水的质量为:100g-20g=80g即80ml;
(3)在量取水的操作中,当水面接近所需刻度时,应改用胶头滴管加水至所需刻度;标签上的内容是:

(4)用排水法收集满氧气后,接下来的操作是在水面下用玻璃片盖住集气瓶口,然后将集气瓶移出水面,正放在桌面上;
故答案为:(1)2KMnO4
| ||
(2)催化作用;20;80;(3)H;

(4)在水面下用玻璃片盖住集气瓶口.
点评:本题考查了实验室制气体的原理书写、发生装置及仪器的选择以及溶液的配制、实验的注意事项等,综合性比较强.本题型要充分利用题目给出的信息及要求逐一完成.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
 (2013?泉州质检)妈妈为小志的十六岁生日聚会准备了很多物品,其中蕴含着丰富的化学知识,请回答:
(2013?泉州质检)妈妈为小志的十六岁生日聚会准备了很多物品,其中蕴含着丰富的化学知识,请回答:
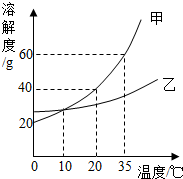 (2013?泉州)如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )
(2013?泉州)如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )