题目内容
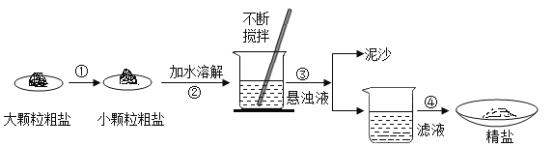
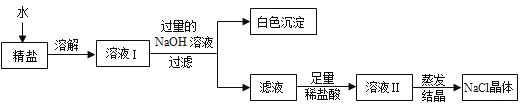
【题目】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

(1)工业生产中,制备NH3的化学方程式是_____。
(2)反应①的另一种产物是配制石灰乳的主要原料之一,其俗名为_____,常用作_____,配制石灰乳时发生的化学方程式为_____。
(3)反应③的化学方程式为_____。
(4)整个生产过程中可循环利用的物质是_____。
【答案】N2+3H2![]() 2NH3 生石灰 干燥剂 CaO+H2O=Ca(OH)2 2NaHCO3
2NH3 生石灰 干燥剂 CaO+H2O=Ca(OH)2 2NaHCO3![]() Na2CO3+H2O+CO2↑ NH3、CO2
Na2CO3+H2O+CO2↑ NH3、CO2
【解析】
(1)氢气与氮气在一定条件下反应生成氨气,化学方程式是:N2+3H2![]() 2NH3;
2NH3;
(2)贝壳的主要成分是碳酸钙,在高温的条件下分解为氧化钙和二氧化碳,氧化钙是配制石灰乳的主要原料之一,其俗名为生石灰,常用作干燥剂,与水反应生成氢氧化钙;化学方程式是:CaO+H2O=Ca(OH)2;
(3)反应③是碳酸氢钠在加热的条件下分解为碳酸钠、水和二氧化碳;化学方程式是:2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(4)通过分析反应原理可知,氨气、二氧化碳既是反应物,也是生成物,所以整个流程中可以循环利用的物质是NH3、CO2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目