题目内容
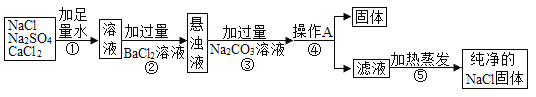
【题目】请结合以下图示,回答问题。
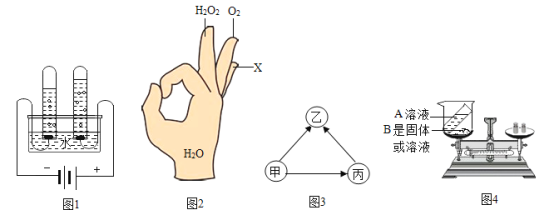
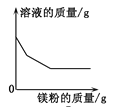
(1)如图1所示,电解水的实验中正极与负极产生气体的质量比为____。
(2)如图2所示,小明用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本反应类型直接生成水(如图中的H2O2、O2),X不能选择下列A、B、C、D4种物质中的____(填序号)
ACuO BH2CO3 CC2H5OH DCa(OH)2
(3)如图3所示,“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是____(用“甲、乙、丙”表示)。
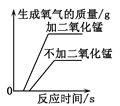
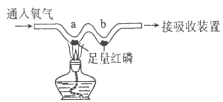
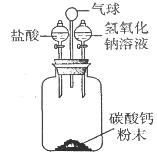
(4)如图4所示,某同学用此装置验证质量守恒定律的实验,下列药品不能达到该实验目的的是____(填序号)。
A 火碱和稀盐酸反应 B 铁和稀盐酸反应
C 铁和硝酸锌溶液反应 D 硫酸和氯化钠溶液
【答案】8:1 C 甲>丙>乙 BCD
【解析】
(1)电解水时正极生成氧气,负极生成氢气,根据反应的化学方程式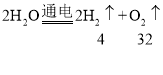 ,可以求出生成氧气和氢气的质量比为:32:4=8:1;
,可以求出生成氧气和氢气的质量比为:32:4=8:1;
(2)A、CuO和酸或者氢气反应都能生成水,和酸反应是复分解反应,和氢气反应是置换反应,都属于基本反应类型,不符合题意;
B、碳酸分解生成水和二氧化碳,该反应属于分解反应,属于基本反应类型,不符合题意;
C、酒精和氧气在点燃的条件下生成二氧化碳和水,不是基本反应类型,符合题意;
D、稀盐酸与氢氧化钙反应生成氯化钙和水,属于复分解反应,属于基本反应类型,不符合题意。故选C。
(3)由图中金属与盐溶液的反应关系可知,金属甲能把金属丙从其盐溶液中置换出来,说明金属甲的活动性比丙强;金属丙能把金属乙从其盐溶液中置换出来,说明金属丙的活动性比乙强;因此三种金属的活动性由弱到强的顺序为:甲>丙>乙。
(4)A、氢氧化钠溶液和稀盐酸反应生成氯化钠和水,可以验证质量守恒定律,不符合题意;
B、铁与稀盐酸反应生成氯化亚铁和氢气,有气体生成应在密闭环境中进行,本装置不可以验证质量守恒定律,符合题意;
C、铁和硝酸锌溶液不反应,不可以验证质量守恒定律,符合题意;
D、硫酸和氯化钠溶液不反应,不可以验证质量守恒定律,符合题意。故选BCD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
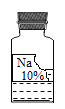
小学生10分钟应用题系列答案【题目】实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)。小强和小华同学很感兴趣,决定对其成分进行探究。
(提出问题)这瓶试剂可能是什么溶液呢?
(交流讨论)根据受损标签的情况判断,这瓶试剂不可能是____。(填序号)
A 酸 B 碱 C 盐
(查阅资料)Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3。
ⅡNa2CO3和NaHCO3的水溶液都呈碱性。
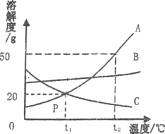
Ⅲ室温(![]() )时,测定四种物质的溶解度数据如下:
)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是___。
(作出猜想)①可能是NaCl;②可能是Na2CO3;③可能是____。
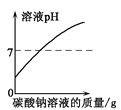
(实验探究)(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH7,则这瓶试剂不可能是____。
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验。
实验步骤 | 实验现象 | 结论及化学方程式 |
①取少量溶液于试管中,滴加____。 | 产生大量气泡 | 反应的化学方程式:___。 |
②把产生的气体通入澄清的石灰水中。 | 澄清的石灰水变浑浊 | 猜想②正确。反应的化学方程式:____。 |
(拓展延伸)请你选择与小强不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择的试剂是____。