题目内容
据图回答:
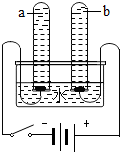
(1)认真观察A、B两装置,写出B装置中发生反应的化学符号表达式______,水中氢元素和氧元素的质量比为______;用分子和原子的观点分析比较A装置和B装置在试验过程中水的变化情况______.
(2)根据水电解的实验回答:①与电源______极(填“正”或“负”)相连的一端产生氢气的体积为100mL时,另一端产生的氧气的体积约为______mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为______g,氢气的质量为______g.
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.你认为可能的原因是(答一条即可)______.

(1)认真观察A、B两装置,写出B装置中发生反应的化学符号表达式______,水中氢元素和氧元素的质量比为______;用分子和原子的观点分析比较A装置和B装置在试验过程中水的变化情况______.
(2)根据水电解的实验回答:①与电源______极(填“正”或“负”)相连的一端产生氢气的体积为100mL时,另一端产生的氧气的体积约为______mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为______g,氢气的质量为______g.
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.你认为可能的原因是(答一条即可)______.

(1)B装置为电解水,水在通电条件下分解成氢气和氧气,反应的化学方程式为H2O
H2+O2;根据水的化学式H2O,水中氢元素和氧元素的质量比=(1×2):16=1:8;
A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
(2)①与电源负极相连的一端产生的是氢气,正极产生氧气,且氢气与氧气的体积比为2:1,故氢气体积为100mL时,另一端产生的氧气的体积约为50mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为50mL×10-3×1.43g/l=0.0715g;氢气的质量为100mL×0.09g/L=0.009g;
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.可能的原因是氧气在水中的溶解能力比氢气大(或产生的氧气会与金属电极发生氧化反应,从而消耗一部分氧气).
故答案为:(1)H2O
H2+O2;1:8;A中的水分子本身没有改变,改变的是分子之间的间隔;B中的水分子发生了改变,变成了氢气分子和氧气分子;
(2)①负;50;②0.0715;0.009;
③氧气比氢气更易溶于水或氧气的氧化性很强,与金属电极发生了氧化反应,消耗了一部分氧气.
| 通电 |
A装置对水加热,水分子间间隔变大,水由液体变成气体,水分子本身并没有发生改变;B装置电解水,水分子变成了氢分子和氧分子,分子本身改变;
(2)①与电源负极相连的一端产生的是氢气,正极产生氧气,且氢气与氧气的体积比为2:1,故氢气体积为100mL时,另一端产生的氧气的体积约为50mL.
②若在此条件下,氢气的密度为0.09g/L,氧气的密度为1.43g/L.则生成的这些氧气的质量为50mL×10-3×1.43g/l=0.0715g;氢气的质量为100mL×0.09g/L=0.009g;
③晓露同学在实验时发现生成的氢气与氧气的体积比约大于理论比值.可能的原因是氧气在水中的溶解能力比氢气大(或产生的氧气会与金属电极发生氧化反应,从而消耗一部分氧气).
故答案为:(1)H2O
| 通电 |
(2)①负;50;②0.0715;0.009;
③氧气比氢气更易溶于水或氧气的氧化性很强,与金属电极发生了氧化反应,消耗了一部分氧气.

练习册系列答案
相关题目