题目内容
【题目】某兴趣小组的同学从实验室收集到一桶含有 FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
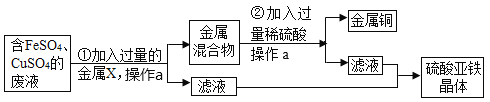
请你根据流程回答下列问题:
(1)操作a的名称是______________。
(2)步骤①中,金属X是_____________,该反应的化学方程式为_____________。
(3)步骤②中,加入过量稀硫酸的目的是_____________。
【答案】过滤 铁 Fe+CuSO4═FeSO4+Cu 除去铜中的铁
【解析】
(1)结合实验方案,可知操作a的名称是过滤;
(2)由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入“铁”将铜离子转化为铜单质。故该反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
(3)因为步骤①中,金属铁过量,故步骤②中,加入过量稀硫酸的目的是除去铜中的铁。

练习册系列答案
相关题目
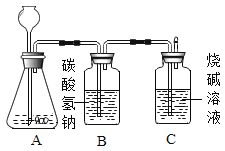
【题目】化学兴趣小组为测定大理石中碳酸钙的含量,如下图所示:将过量的稀盐酸加入到20g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量,结果如下表所示:
时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
C增加质量/C | 0 | 3.0 | 5.0 | 6.0 | 6.6 | x | 6.6 |
(1)(1)上表中,第10分钟时,x=___;
(2)(2)计算大理石样品中碳酸钙的质量分数(写出计算过程) ___
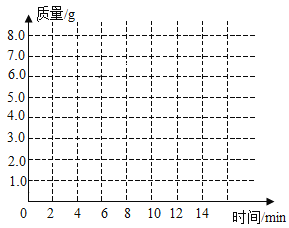
(3)(3)请在下图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线: ___;
(4)B中所装药品为饱和碳酸氢钠溶液,作用是吸收可能挥发的HCl气体,你认为没有B,测量结果会____.(填“偏高”或“偏低”)。