题目内容
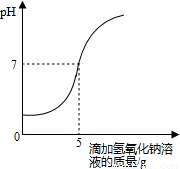
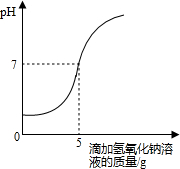 硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.请根据实验计算,该污水中硫酸的溶质质量分数是多少?
硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.请根据实验计算,该污水中硫酸的溶质质量分数是多少?
分析:已知中性溶液的ph值为7,由图示数据可知,向污水中滴加氢氧化钠溶液至5g时,与硫酸完全反应.利用氢氧化钠与硫酸反应的化学方程式和氢氧化钠的质量,列出比例式,可计算出样品中H2SO4的质量;然后根据溶质质量分数公式计算即可.
解答:解:设样品中H2SO4的质量为x,
2NaOH+H2SO4=Na2SO4+2H2O
80 98
5g×4%,x
∴
=
,
解之得:x=0.245g,
则该污水中硫酸的溶质质量分数是:
×100%=2.45%.
答:该污水中硫酸的溶质质量分数是2.45%.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
5g×4%,x
∴
| 80 |
| 98 |
| 5g×4% |
| x |
解之得:x=0.245g,
则该污水中硫酸的溶质质量分数是:
| 0.245g |
| 10g |
答:该污水中硫酸的溶质质量分数是2.45%.
点评:本题是有关化学方程式和溶质质量分数的简单计算.解题时要注意格式和步骤.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
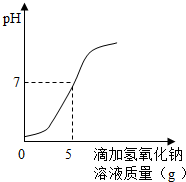 硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数某学习小组做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为8%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.(污水中其它物质不与氢氧化钠反应.
硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数某学习小组做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为8%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.(污水中其它物质不与氢氧化钠反应.