题目内容
【题目】水是生命之源,“爱惜水、保护水”是每个公民的义务和责任. 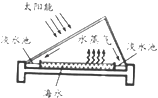
(1)海水淡化是获取淡水的方法之一,用如图方法获得淡水的过程中发生的是变化(填写“物理”或“化学”);
(2)今年4月25日尼泊尔境内发生地震,高铁酸钾(K2FeO4)可用于灾区饮用水的净化,制备K2FeO4的化学反应方程式为:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,X的化学式为 , K2FeO4中Fe元素的化合价为 .
(3)污水处理是防止水污染的重要措施之一,某工厂甲、乙两车间产生的污水中各含有以下四种物质中的两种:Ba(NO3)2 , KOH,K2SO4 , HNO3 , 用石蕊试液和氯化钡溶液分别对两车间污水进行检测,现象如下表:
| 石蕊试液 | 氯化钡溶液 |
甲车间 | 变蓝色 | 产生白色沉淀 |
乙车间 | 变红色 | 无明显现象 |
则甲车间产生的污水含有上述四种物质中的 , 工厂决定将两车间产生的污水排入反应池内充分反应后再排放,写出发生反应的中和反应的化学方程式 , 若反应池内各物质均恰好完全反应,排放液中的溶质是(填写物质名称).
【答案】
(1)物理
(2)KCl;+6
(3)KOH,K2SO4;KNO3+KOH═KNO3+H2O;KNO3
【解析】解:(1)如图方法获得淡水是水的蒸发获取的,发生的是物理变化,故填:物理;(2)2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,反应前含有12个Fe原子,16个H原子,16个O原子,6个Cl原子,反应后含有6个K原子,16个H原子,16个O原子,故6X中含有6个K原子,6个C磷原子,故X的化学式为KCl,K2FeO4中钾元素的化合价为+1,O元素的化合价为﹣2,设Fe元素的化合价为x,则有:(+1)×2+x+(﹣2)×4=0.x=+6,故填:KCl,+6.(3)
| 石蕊试液 | 氯化钡溶液 |
甲车间 | 变蓝色 | 产生白色沉淀 |
乙车间 | 变红色 | 无明显现象 |
根据表格提供的知识,甲车间能使石蕊试液变蓝,故甲车间的废液呈碱性,氢氧化钾呈碱性,故甲中含有氢氧化钾,乙中含有硝酸,由于氯化钡能与硫酸钾反应产生沉淀,故甲中含有硫酸钾,硫酸钾能与硝酸钡反应产生沉淀,故硝酸钡来自乙车间,故甲车间产生的污水含有上述四种物质中的KOH、K2SO4 , 发生反应的中和反应的化学方程式 KNO3+KOH═KNO3+H2O,若反应池内各物质均恰好完全反应,排放液中的溶质是KNO3 , 故填:KNO3+KOH═KNO3+H2O,KNO3 .
【考点精析】解答此题的关键在于理解质量守恒定律及其应用的相关知识,掌握①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.



