题目内容
(6分)根据所学知识回答下列问题:
A B C D E
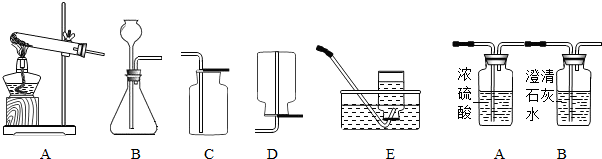
(1)实验室用高锰酸钾制取氧气的化学方程式是 ,所选用的发生装置是 (填字母),用C装置收集氧气后,验满的方法是 。
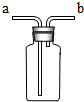
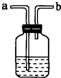
(2)图F所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是 ,植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响。
F G
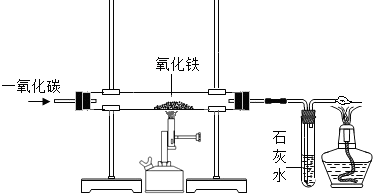
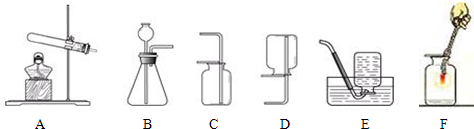
(3)做空气中氧气含量测定的实验装置如G图所示。下列有关说法正确的是 (填字母)。
| A.选用红磷是因为反应可以耗尽氧气,生成固态的五氧化二磷 |
| B.燃烧匙中的红磷可以换成硫和木炭 |
| C.燃烧匙中的红磷越多,水位上升越高 |
| D.本实验可以证明空气含有N2、O2、CO2和稀有气体 |
31.(6分,每空l分。)
(1) 2KMnO4 K2MnO4+MnO2+ O2↑, A,将带火星的木条放在集气瓶口,若木条复燃则已满。
K2MnO4+MnO2+ O2↑, A,将带火星的木条放在集气瓶口,若木条复燃则已满。
(2) 防止CO2溶于水,没有。
(3) A
解析试题分析:(1)实验室用高锰酸钾制取氧气的化学方程式是2KMnO4 K2MnO4+MnO2+ O2↑,所选用的发生装置是加热固体制取气体的装置,选A;用C装置即向上排空气法收集氧气后,验满的方法是将带火星的木条放在集气瓶口,若木条复燃则已满。
K2MnO4+MnO2+ O2↑,所选用的发生装置是加热固体制取气体的装置,选A;用C装置即向上排空气法收集氧气后,验满的方法是将带火星的木条放在集气瓶口,若木条复燃则已满。
(2)图F所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的是防止CO2溶于水,植物油上方原有的空气对实验的结果没有明显影响。
(3)用燃烧法测定空气中氧气的体积分数,要注意几点:1、装置不能漏气;2、红磷要足量;3、装置冷却后才能打开止水夹;4、可燃物在装置内燃烧后不能生成别的气体。空气中含有约1/5体积的氧气,实验结束后,进入装置内的水约占1/5体积。
考点:实验室制取氧气的反应原理;装置选择;验满氧气;燃烧法测定空气中氧气的体积分数。
点评:氧气是常考的重要知识点,同学们务必要掌握。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案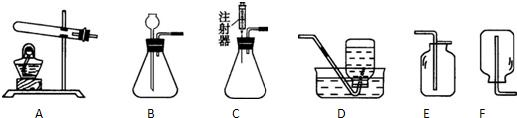
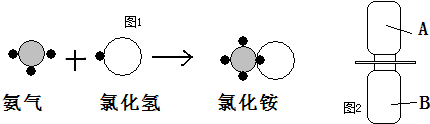
 表示的是
表示的是 ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图1表示:
”表示氯原子,上述反应过程可用图1表示: