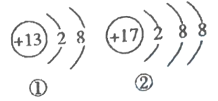题目内容
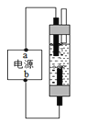
【题目】下图是实验室制取某些常见气体所使用的一些装置和仪器。
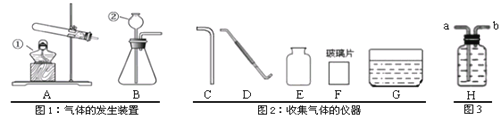
(1)写出图中标号仪器的名称:②___________。
(2)实验室用A装置制取氧气,反应的符号表达式为__________, 收集较纯氧气通常选择图2中的________(填编号)仪器进行组合。若要测量生成氧气的体积,应将图3中_______(填“a”或“b”)导管与量筒相连。
(3)制取氧气的反应结束后,若要将试管内固体剩余物中的MnO2回收利用,需要按照以下流程进行分离:
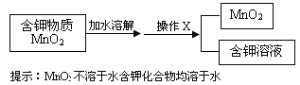
操作X的名称是____,在实验室中进行该操作时用到的玻璃仪器有漏斗、烧杯、_______。
(4)实验室用过氧化氢溶液制取氧气,反应的符号表达式为_______。下表是某兴趣小组的同学探究影响过氧化氢分解速率因素的相关实验数据:
实验 序号 | H2O2溶 液浓度% | H2O2溶液体积mL | 温度℃ | MnO2的 用量/g | 收集氧气 的体积/mL | 反应所需 的时间/s |
甲 | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
乙 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
丙 | 30 | 5 | 35 | 0 | 2 | 49.21 |
丁 | 30 | 5 | 55 | 0 | 2 | 10.76 |
①通过实验甲和乙对比可知,过氧化氢的分解速率与___________有关;
②从实验______和______(填实验序号)对比可知,过氧化氢的分解速率与温度的关系是______________;
③通过上述实验______(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率。
【答案】长颈漏斗。 KMnO4![]() K2MnO4+MnO2+O2, DEFG, a 过滤, 玻璃棒 H2O2
K2MnO4+MnO2+O2, DEFG, a 过滤, 玻璃棒 H2O2![]() H2O + O2 H2O2溶液的浓度 丙 丁 温度越高,分解速率越快 不能
H2O + O2 H2O2溶液的浓度 丙 丁 温度越高,分解速率越快 不能
【解析】
(1)②是长颈漏斗。(2)试管口放棉花团是用高锰酸钾制取氧气,高锰酸钾发生分解反应生成锰酸钾、二氧化锰、氧气。用排水法收集的气体较纯净,用排水法收集氧气用到的玻璃仪器有导气管、集气瓶、毛玻璃片、水槽。要测量生成氧气的体积,后面要连接一个量筒,量筒中水的体积等于收集到的氧气的体积,当装置中的水减少时,易从a导气管导出,所以a与量筒连接。(3)经过过滤可将固体与液体分离。过滤时用到的玻璃仪器有漏斗、烧杯、玻璃棒。(4)过氧化氢溶液在二氧化锰作催化剂的条件下发生分解反应生成水、氧气。①实验甲和实验乙只是过氧化氢溶液的浓度不同,实验乙中过氧化氢溶液的浓度大,收集4ml氧气所用时间最短,所以过氧化氢的分解速率与浓度有关。②实验丙与实验丁只是温度不同,实验丙温度高,收集2ml氧气所用时间短,所以温度越高,分解速率越快。说明使用MnO2可以加快H2O2溶液反应速率,必须做对比实验,一个实验中加入二氧化锰,一个实验中不加入二氧化锰,其它条件完全相同。

 寒假学与练系列答案
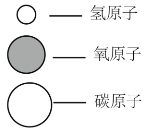
寒假学与练系列答案【题目】某纯净物 A 在物质 B 中充分燃烧,发生反应:A+3B![]() 2C+3D(部分微观示意图如下所示)。下列说法不正确的是
2C+3D(部分微观示意图如下所示)。下列说法不正确的是
物质 | A | B | C | D |
|
分子示意图 | ? |
|
|
|
A. A 物质中含有碳、氢、氧三种元素
B. A 物质中的碳、氢原子个数比为 2:3
C. A 物质具有可燃性,但一定不是氧化物
D. 该反应既不是化合反应,也不是分解反应