题目内容
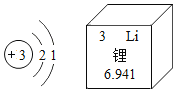
【题目】下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题:

(1)磷原子的核电荷数是__________。
(2)硫原子在化学反应中易形成_____(填“阳离子”或“阴离子”),其符号为________。请你写出钠原子与硫原子反应形成的化合物的化学式________。
(3)质子数为9的氟原子与上述表格中的______________原子的化学性质相似。
(4)从原子结构角度分析,上述元素位于同一周期的原因是____________。
【答案】15 阴离子 S2- Na2S 氯(或者Cl) 电子层数相同
【解析】
(1)由图中信息可知,磷原子的质子数是15,原子中,质子数=核电荷数,故磷的核电荷数为15;
(2)带正电荷的离子叫阳离子,带负电荷的离子为阴离子。硫原子在化学反应中易得电子形成阴离子,其符号为S2-;元素化合价的数值与离子所带电荷的数值相等,正负号相同。钠原子与硫原子反应形成的化合物的化学式Na2S;
(3)具有稳定结构的原子彼此化学性质相似,不是稳定结构的原子,最外层电子数相同的化学性质相似。质子数为9的氟原子与上述表格中的氯原子的化学性质相似;
(4)在元素周期表中,元素的周期数等于原子的核外电子层数,从原子结构角度分析,上述元素位于同一周期的原因是电子层数相同,都有三个电子层,都在第三周期。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】下列图像与对应的实验相符合的是
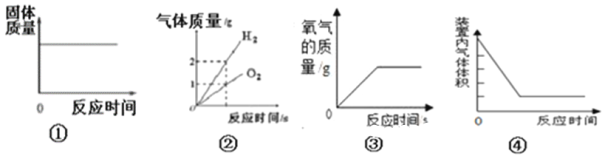
A. 图①是将一定质量的红磷放在盛有氧气的密闭容器中燃烧
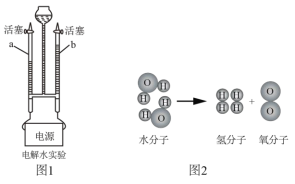
B. 图②是水的电解
C. 图③是实验室用过氧化氢溶液制取氧气
D. 图④测定空气中氧气的含量时装置内气体体积
【题目】以下是某小朋友血液中某些元素检测结果的报告单(部分),回答以下问题:
序号 | 检测项目 | 结果 | 参考值 |
1 | 锌 | 7.7 | 11~22 μmolL-1 |
3 | 铁 | 17.8 | 9.0~21.5 μmolL-1 |
4 | 钙 | 2.5 | 2.2~2.7 μmolL-1 |
6 | 铅 | 0.28 | 0~0.48 μmolL-1 |
(1)该小朋友缺乏的微量元素是_____ (填元素符号);缺乏此元素会_______________ 。
(2)根据检测结果,医生建议她每天补充10mg的锌,该小朋友的爸爸给她买了补锌剂(标签如图)。

葡萄糖酸锌中含有______种金属元素,试通过计算说明该小朋友每天一共应该吃______ 片。
(3)该小朋友的妈妈认为葡萄糖酸锌片是营养补剂,多吃几片没关系.请你评价这一观点,并说出理由___________ 。
【题目】下图是实验室制取某些常见气体所使用的一些装置和仪器。
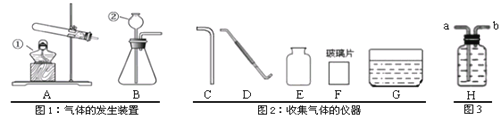
(1)写出图中标号仪器的名称:②___________。
(2)实验室用A装置制取氧气,反应的符号表达式为__________, 收集较纯氧气通常选择图2中的________(填编号)仪器进行组合。若要测量生成氧气的体积,应将图3中_______(填“a”或“b”)导管与量筒相连。
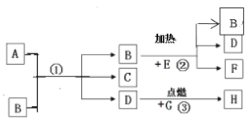
(3)制取氧气的反应结束后,若要将试管内固体剩余物中的MnO2回收利用,需要按照以下流程进行分离:
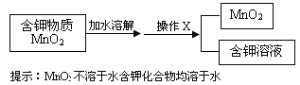
操作X的名称是____,在实验室中进行该操作时用到的玻璃仪器有漏斗、烧杯、_______。
(4)实验室用过氧化氢溶液制取氧气,反应的符号表达式为_______。下表是某兴趣小组的同学探究影响过氧化氢分解速率因素的相关实验数据:
实验 序号 | H2O2溶 液浓度% | H2O2溶液体积mL | 温度℃ | MnO2的 用量/g | 收集氧气 的体积/mL | 反应所需 的时间/s |
甲 | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
乙 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
丙 | 30 | 5 | 35 | 0 | 2 | 49.21 |
丁 | 30 | 5 | 55 | 0 | 2 | 10.76 |
①通过实验甲和乙对比可知,过氧化氢的分解速率与___________有关;
②从实验______和______(填实验序号)对比可知,过氧化氢的分解速率与温度的关系是______________;
③通过上述实验______(填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率。