题目内容
【题目】将等质量的镁和铁分别放入等质量、等溶质的质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是
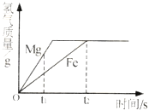
A.反应结束后镁有剩余
B.反应消耗盐酸的总质量相等
C.0~t1时段,与镁反应的HCl的质量大
D.0~t2时段,参加反应的镁的质量与铁相等
【答案】D
【解析】
试题分析:解答图像类的题目抓住“三点一走势”,即首先看清楚横、纵坐标各表示的量,然后从起始点、转折点、终点还有量的变化趋势来进行分析解答,A、根据化学方程式:Mg+ 2HCl === MgCl2 + H2↑中Mg和氢气的质量关系24:2,Fe + 2HCl === FeCl2 + H2↑中Fe和氢气的质量关系56:2,结合产生的氢气质量相等,所需消耗铁的质量比镁多,反应结束后镁有剩余,正确,B、金属与酸反应生成的氢气全部来自酸中的氢,由于最终产生的氢气质量相等,故反应消耗盐酸的总质量相等,正确,C、根据图像:0~t1时段,与镁反应的HCl的质量大,正确,D、0~t2时段,表示两个反应都结束,最终产生的氢气质量相等,故参加反应的镁的质量与铁不相等,错误,故选D

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目