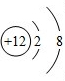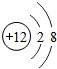题目内容
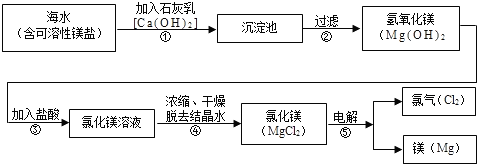
镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.海水提镁是国际上的主要趋势,工业流程图如下;
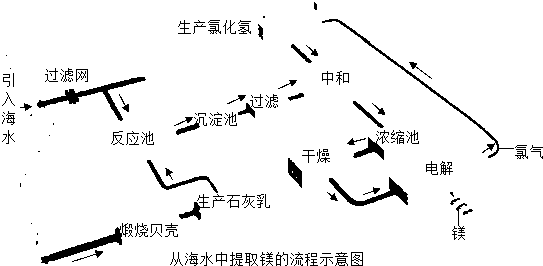
其步骤为:
Ⅰ.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O
Ⅳ.将MgCl2?6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
①写出步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ的有关化学方程式,并注明基本反应类型:
Ⅰ、
Ⅱ、
Ⅲ、
Ⅳ、
②步骤Ⅳ在实验室中进行蒸发结晶得到MgCl2需要的主要仪器有

其步骤为:
Ⅰ.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O
Ⅳ.将MgCl2?6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
①写出步骤Ⅰ、Ⅱ、Ⅲ、Ⅳ的有关化学方程式,并注明基本反应类型:
Ⅰ、
CaCO3
CaO+CO2↑、CaO+H2O═Ca(OH)2
| ||
CaCO3
CaO+CO2↑、CaO+H2O═Ca(OH)2
、反应类型:
| ||
分解反应、化合反应
分解反应、化合反应
Ⅱ、
MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
、反应类型:复分解反应
复分解反应
Ⅲ、
Mg(OH)2+2HCl=MgCl2+2H2O
Mg(OH)2+2HCl=MgCl2+2H2O
、反应类型:复分解反应
复分解反应
Ⅳ、
MgCl2?6H2O
MgCl2+6H2O
| ||
MgCl2?6H2O
MgCl2+6H2O
、反应类型:
| ||
分解反应
分解反应
②步骤Ⅳ在实验室中进行蒸发结晶得到MgCl2需要的主要仪器有
蒸发皿
蒸发皿
、玻璃棒
玻璃棒
、酒精灯、带铁圈的铁架台、坩埚钳等.分析:根据反应物和生成物及其质量守恒定律可以书写化学方程式;根据化学方程式可以判断反应类型;在实验室中进行蒸发操作需要的主要仪器有蒸发皿、玻璃棒、酒精灯、带铁圈的铁架台、坩埚钳等
解答:解:(1)①Ⅰ贝壳煅烧成生石灰的化学方程式为:CaCO3
CaO+CO2↑是一种变多种,属于分解反应.生石灰溶于水制成石灰乳,方程式为:CaO+H2O═Ca(OH)2反应物是两种,生成物是一种,属于化合反应;
Ⅱ、将石灰乳加入到海水反应池中,与氯化镁反应生成氢氧化镁沉淀,经过沉降、过滤得到Mg(OH)2,方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,是两种化合物相互交换成分生成另外两种化合物,属于复分解反应;
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O.反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.属于复分解反应;
Ⅳ.将MgCl2?6H2O在一定条件下加热得到无水MgCl2方程式为:MgCl2?6H2O
MgCl2+6H2O 属于分解反应;
②.在实验室中进行蒸发操作需要的主要仪器有蒸发皿、玻璃棒、酒精灯、带铁圈的铁架台、坩埚钳等.
故答案为Ⅰ、
CaCO3
CaO+CO2↑、CaO+H2O═Ca(OH)2 分解反应、化合反应
MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
复分解反应
Ⅲ、Mg(OH)2+2HCl=MgCl2+2H2O
复分解反应
Ⅳ、MgCl2?6H2O
MgCl2+6H2O 分解反应
②蒸发皿玻璃棒
| ||
Ⅱ、将石灰乳加入到海水反应池中,与氯化镁反应生成氢氧化镁沉淀,经过沉降、过滤得到Mg(OH)2,方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2,是两种化合物相互交换成分生成另外两种化合物,属于复分解反应;
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2?6H2O.反应的化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O.属于复分解反应;
Ⅳ.将MgCl2?6H2O在一定条件下加热得到无水MgCl2方程式为:MgCl2?6H2O
| ||
②.在实验室中进行蒸发操作需要的主要仪器有蒸发皿、玻璃棒、酒精灯、带铁圈的铁架台、坩埚钳等.
故答案为Ⅰ、
CaCO3
| ||
MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
复分解反应
Ⅲ、Mg(OH)2+2HCl=MgCl2+2H2O
复分解反应
Ⅳ、MgCl2?6H2O
| ||
②蒸发皿玻璃棒
点评:解答本题要掌握化学方程式的书写方法和反应类型的判断方法

练习册系列答案
相关题目
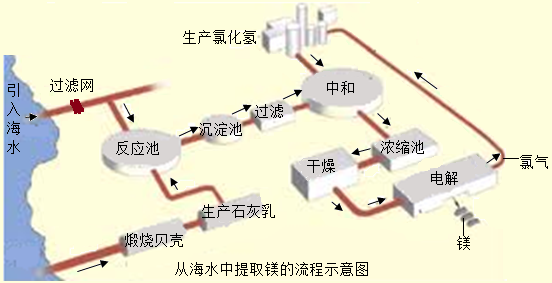
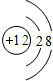 该图表示(填序号)
该图表示(填序号)