题目内容
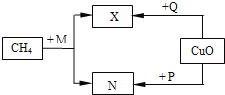
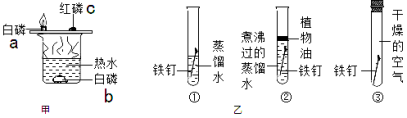
【题目】(7分)某化学兴趣小组在探究Mg、Fe、Cu的性质时进行了如下图所示实验。

(1)实验一中,发生反应的化学方程式为 。
(2)实验二中,将实验一所得的物质倒入烧杯中,发现烧杯内的红色固体明显增多,充分反应后过滤。
①滤液中所含金属离子的成分可能是 (选填字母)。
A.Mg2+ B.Mg2+和Fe2+
C.Cu2+和Fe2+ D.Mg2+、Fe2+和Cu2+
②确定滤渣成分的实验方案如下:
操 作 | 现 象 | 结 论 |
取少量滤渣于试管中, 滴加 | 无明显现象 | 滤渣为 |
滤渣为 |
【答案】(1)Fe+CuSO4 Cu+FeSO4(2)① BD
②(合理答案均可)
操 作 | 现 象 | 结 论 |
稀盐酸 | Cu | |
产生气泡,溶液变为浅绿色 | Fe和Cu |
【解析】
试题分析:(1)反应物是铁和硫酸铜,生成物是铜和硫酸亚铁,已经平了改成等号即可;铁能与硫酸铜反应说明铁排在了铜的前面,铁不能与硫酸镁反应,说明铁排在了镁的后面;(2)将实验一后①、②试管内的物质倒入烧杯中,发现烧杯内的红色固体明显增多,说明铁在置换铜,一段时间后过滤.滤渣中一定含有的物质是铜,可能有的物质就是铁,铁可能反应完了,也可能没反应完有剩余;由于铁能与盐酸反应生成氢气,所以取少量滤渣于试管中,向其中滴加稀盐酸,有气泡说明含有铁,否则没有铁;由于铁与硫酸镁不反应,所以滤液中一定含有镁离子,又因为通过检验发现铁没有剩余,说明铁参加了反应到了溶液中以亚铁离子的形式存在,铜离子有没有不能确定,可能有可能没有

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目