题目内容
【题目】从分子的角度分析并解释下列事实,不正确的是
选项 | 事 实 | 解 释 |
A | 碘酒是混合物 | 由不同种分子构成 |
B | 端午时节粽飘香 | 分子在不断运动着 |
C | 气体受热膨胀 | 温度升高,分子自身体积增大 |
D | 固体碘受热升华 | 碘分子间的间隔变大 |
A. A B. B C. C D. D
【答案】C
【解析】试题分析:气体受热膨胀是因为构成物质的分子间有间隔,间隔随温度的升高而增大,分子本身不变。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案【题目】以下是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
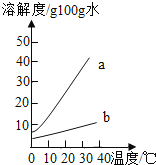
(1)要除去Na2CO3固体中的少量NaHCO3,应采用的物理方法是 (填写编号).
①冷却热饱和溶液 ②蒸发溶剂 ③溶解过滤
(2)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O→2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是 .
(3)40℃时的100g Na2CO3的饱和溶液中含有 g溶质,该溶液的溶质质量分数为 %.(计算结果精确到0.1)
(4)若将30%的碳酸钠溶液100g,稀释到10%,需要加水 mL.
(5)在上述(3)的配制过程中,不需要的仪器是(填序号) .
A.托盘天平 B.100mL量筒 C.25mL量筒 D.250mL烧杯
(6)“水的蒸发”和“水的电解”两个实验中水发生变化的本质区别是(从微观视角分析) .
【题目】用科学方法认识和改造物质.请你参与探究并填空:
按照科学认识的过程,科学方法主要蕴含在二个阶段:一是感性认识阶段,主要是为了获得证据,如观察、预测、实验等;二是理性认识(理性思维)阶段,主要是为了形成科学认识,如科学抽象、科学假说,像比较与对比、归纳与演绎等.
在前一阶段的学习中,我们通过实验、观察等手段验证了很多化学反应的发生,运用了“归纳、演绎;比较、对比”等科学的一般方法认识了几种典型的酸、碱、盐.请你运用以上方法认识氯化镁.
(1)用归纳/演绎的方法认识氯化镁的性质
已知下列反应:
HCl+AgNO3═AgCl↓+HNO3
NaCl2+AgNO3═AgCl↓+NaNO2
BaCl2+2AgNO3═2AgCl↓+Ba(NO3)2…
①这组反应能够发生的原因是 .
②由①中得到的规律可以推论“氯化镁溶液也能跟硝酸银溶液反应”,运用的是 的方法.
(2)用实验的方法认识氯化镁的性质
①要验证(1)②中“氯化镁溶液也能跟硝酸银溶液反应”的推论,需进行实验,实验方法是:
实验操作 | 实验现象 | 结论 |
结论:氯化镁溶液能跟硝酸银溶液反应 |
②用实验的方法认识氯化镁的其他性质
实验操作 | 实验现象 | 结论 |
取少量氯化镁溶液于试管中,然后再滴加2﹣3滴紫色石蕊试液,振荡 | 石蕊试液变红 | 结论:氯化镁溶液 |
取少量氯化镁溶液于试管中,然后再滴加氧化钠溶液 | 产生白色沉淀 | 结论: |
(3)用重要的学科实验方法﹣﹣“化学转化法”改造物质
人类利用化学变化,创造出我们所需要的物质,极大地促进了人类社会的发展.工业上以海水为原料,通过一系列化学变化可以得到氯化镁晶体;将无水氯化镁(MgCl2)在熔融状态下,通电后可以得到“国防金属”镁.反应流程如图所示,请从化学视角回答下列问题:
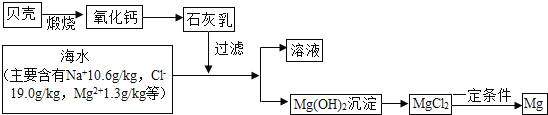
①要使海水中的MgCl2完全转化为沉淀Mg(OH)2,加入石灰乳(主要成分是氢氧化钙)要过量.请同学设计实验确定海水中的MgCl2已全部转化为Mg(OH)2;取上层清液少量于试管中,向其中加入 ,观察到 ,说明海水的MgCl2已全部转化为Mg(OH)2.
②要将沉淀出的氢氧化镁转化为氯化镁,可以选用的试剂是 .
③海水中本来就有氯化镁,请分析从海水中制取MgCl2时,要经历“MgCl2→Mg(OH)2→MgCl2”的转化过程的原因: .
