��Ŀ����
����Ŀ����ͼΪ��XX����Ƭ��Ʒ��ǩͼ������ݱ�ǩ���й���Ϣ������и��⡣

(1)ÿƬ��Ƭ�к���Ԫ�ص���������Ϊ___��
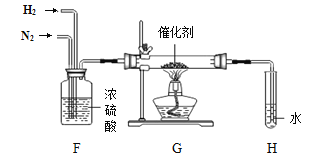
(2)С��ͬѧΪ�ⶨ����̼��Ƶĺ�����ע�Ƿ���ʵ����ȡ��10Ƭ��Ƭ����������С�ձ��У��ټ���50gϡ���ᣬ��T0��T3ʱ��Σ���÷�Ӧʣ����������仯���£�
ʱ�� | T0 | T1 | T2 | T3 |
��Ӧʣ��������(g) | 70 | 65 | 63.4 | 63.4 |
�����ɵĶ�����̼��������___�ˣ�
��ͨ�������жϸø�Ƭ��̼��Ƶĺ�����ע�Ƿ���ʵ___��(д���������)
���𰸡�0.6 6.6 �ø�Ƭ��̼��Ƶĺ�����ע��ʵ
��������
(1) ÿƬ��Ƭ�к�̼���![]() 1.5g����Ԫ�ص�����=̼��Ƶ�����
1.5g����Ԫ�ص�����=̼��Ƶ�����![]() ��Ԫ�ص�����������
��Ԫ�ص�����������
(2) ��T2��T3��Ӧʣ��������(g)��ȣ�˵��̼����Ѿ���ȫ�ֽ⣬�ٸ��������غ㶨�ɣ���ö�����̼��������
�ڸ��ݻ�ѧ����ʽCaCO3+2HCl�TCaCl2+H2O+CO2�������̼��Ƶ��������ٱȽϿ��Ƿ�ÿƬ��Ƭ�к�̼���![]() 1.5g��
1.5g��
(1)ÿƬ��Ƭ�к�̼��Ƶ���������1.5g�����Ը�Ԫ�ص���������Ϊ![]() ��
��
(2)���������غ㶨�ɣ�������̼������Ϊ��2g��10+50g��36.4g��6.6g
��ÿƬ��Ƭ���е�̼��Ƶ�����Ϊx��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
10x 6.6g
![]()
x��1.5g
���ǩ����һ�¡�
��(1)ÿƬ��Ƭ�к���Ԫ�ص���������Ϊ0.6��
(2)�ٶ�����̼��������6.6�ˣ�
�ڸø�Ƭ��̼��Ƶĺ�����ע��ʵ��