题目内容
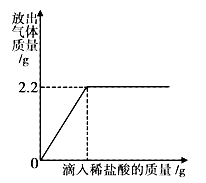
【题目】鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙的质量分数,小华同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取20g放在烧杯里,然后往烧杯中滴加足量的稀盐酸,加入稀盐酸的量与生成气体的量如图所示。试求该鸡蛋壳中钙元素的质量分数。(假设鸡蛋壳中其他物质不与盐酸反应)
【答案】10﹪
【解析】
试题分析:由图像可知最终生成二氧化碳2.2g,由化学方程式可以计算出二氧化碳和碳酸钙的质量比,然后根据由二氧化碳的质量算出碳酸钙的质量,进而计算鸡蛋壳中钙元素的质量分数
解:由图可知:20g鸡蛋壳与稀盐酸完全反应后生成CO2的质量为2.2g
设20g鸡蛋壳中含有CaCO3的质量为X
CaCO3 + 2HCl ══Ca Cl2 + H2O ﹢CO2↑
100 44
X 2.2g
100 ︰ 44 = X :2.2g
X = 100 ×2.2g /44 = 5g
5g CaCO3中钙元素的质量为
5g × 40/100 = 2g
该鸡蛋壳中钙元素的质量分数为
2g /20g × 100﹪ = 10﹪
答:该鸡蛋壳中钙元素的质量分数为10﹪ 。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目