题目内容
【题目】小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体,实验所得数据见下表,请你分析并进行有关计算
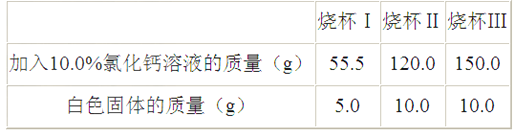
样品中碳酸钠的质量分数是多少(结果精确到0.1%)
【答案】96.4%
【解析】本题考查了含杂质物质的化学反应的有关计算。
由实验数据可知,11.0g样品中的碳酸钠与氯化钙溶液充分反应最多生成10.0g碳酸钙。
(1)设:生成10.0g碳酸钙需要碳酸钠的质量为X
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10.0g
![]() 解得:x=10.6g
解得:x=10.6g
样品中碳酸钠的质量分数=![]() ×100%=96.4%;
×100%=96.4%;
答:样品中碳酸钠的质量分数是96.4%。

练习册系列答案
相关题目