题目内容
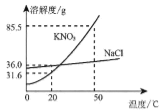
【题目】根据KNO3和NaCl的溶解度曲线,回答下列问题:
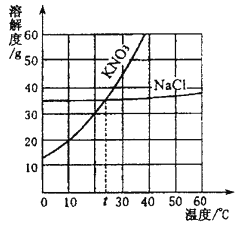
(1)10℃时 KNO3的溶解度_____________(填“>”、“<”或“=”)NaCl的溶解度。
(2)t℃时,将mg KNO3、ngNaCl分别溶解在20mL水中恰好饱和,则m___n(填 “>”、“<”或“=”)。
【答案】< =
【解析】
由KNO3和NaCl的溶解度曲线图可知,硝酸钾的溶解度随温度的升高而增大,氯化钠的溶解度受温度的影响较小。
(1)由KNO3和NaCl的溶解度曲线图可知,10℃时 KNO3的溶解度<NaCl的溶解度。
(2)t℃时,氯化钠的溶解度和硝酸钾的溶解度相同,将mg KNO3、ngNaCl分别溶解在20mL水中恰好饱和,则溶质质量相同,故m=n。

【题目】碳酸氢铵是一种常用的化肥,小组同学对碳酸氢铵进行相关的探究:
[查阅资料] (1)碳酸氢铵是一种白色粒状晶体,有氨味,易溶于水。
(2)氨气具有刺激性气味,极易溶于水,能使湿润的红色石蕊试纸变蓝。
[提出问题]碳酸氢铵有哪些化学性质?
[作出猜想]猜想一:碳酸氢铵能与酸反应;
猜想二:碳酸氢铵能与碱反应;
猜想三:碳酸氢铵易分解。
[设计与实验]
实验操作 | 实验现象 | 实验结论 | |
1 | ______ | 有气泡产生 | 猜想一正确 |
2 | 取少量碳酸氢铵样 品与熟石灰混合研磨 | ____ | 猜想二正确 |
3 |
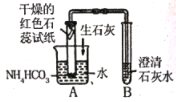
| 红色石蕊试纸变蓝,澄清石灰水变浑浊 | 猜想三正确,B中发生反应的化学方程式 为____ |
[反思] (1)实验3中向水中加入氧化钙的目的是_______。
(2)有同学对实验2的结论提出质疑:碳酸氢铵易分解产生有刺激性气味的气体,研磨会使温度升高,能加快碳酸氢铵分解,所以实验2的结论不严谨。
[补充探究]有同学为了进一步验证猜想二,进行如下实验:
实验操作 | 实验现象 |
①将碳酸氢铵溶液加入到氢氧化钙溶液中 | 有白色沉淀生成,但没有气体逸出 |
②将碳酸氢铵溶液加入到氢氧化钠溶液中 | 有刺激性气味的气体生成 |
[分析]根据常见酸、碱、盐的溶解性分析,①实验中生成的白色沉淀是____,实验中没有气体逸出可能的原因是_______。
[实验结论]三个猜想均正确。
[拓展应用]保存或使用碳酸氢铵时,需注意_______(写出一点)。