��Ŀ����
����Ŀ��������ͼװ�ã��ش������й����⣺
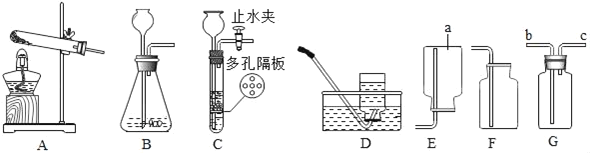
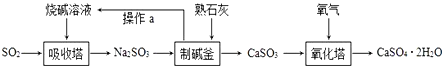
��1��װ��ͼ������a������Ϊ_____��
��2�����ü�������غͶ���������ȡ�����Ļ�ѧ����ʽ��_____����ѡ�õķ���װ�ú��ռ�װ�õ������_____��Aװ���Թܿ������µ�Ŀ����_____��
��3������Gװ�ò����ſշ��ռ�����������Ӧ��_____������ѡ��b����c����
��4����ȡ������̼��Ӧ�Ļ�ѧ����ʽ��_____�����ѡ�õķ���װ����_____����װ������һ����ѡ�õ�װ����ȣ�����Ҫ�ŵ���_____��
���𰸡�����ƿ 2KClO3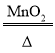 2KCl+3O2�� AD��AF ��ֹҩƷ��ˮ���ڼ���ʱ���ˮ�����ڹܿ�������������ʹ�Թ����� c CaCO3+2HCl��CaCl2+H2O+CO2�� C ���Կ��Ʒ�Ӧ�ķ�����ֹͣ
2KCl+3O2�� AD��AF ��ֹҩƷ��ˮ���ڼ���ʱ���ˮ�����ڹܿ�������������ʹ�Թ����� c CaCO3+2HCl��CaCl2+H2O+CO2�� C ���Կ��Ʒ�Ӧ�ķ�����ֹͣ
��������
��ȡװ�ð������ȺͲ���������֣������˫��ˮ�Ͷ��������������Ͳ���Ҫ���ȣ�����ø�����ػ����������������Ҫ���ȡ��������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ����Թܿ���������бԭ���ǣ���ֹҩƷ��ˮ���ڼ���ʱ���ˮ�����ڹܿ�������������ʹ�Թ����ѡ�
��1������ƿ���ռ������������
��2����������������������Ҫ���ȣ�������ڶ��������������ͼ��ȵ������������Ȼ��غ���������ѧ����ʽΪ2KClO3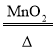 2KCl+3O2�����������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ���ѡ�õ�װ��ΪAD��AF���Թܿ���������бԭ���ǣ���ֹҩƷ��ˮ���ڼ���ʱ���ˮ�����ڹܿ�������������ʹ�Թ����ѡ�
2KCl+3O2�����������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ���ѡ�õ�װ��ΪAD��AF���Թܿ���������бԭ���ǣ���ֹҩƷ��ˮ���ڼ���ʱ���ˮ�����ڹܿ�������������ʹ�Թ����ѡ�
��3������Gװ�ò����ſշ��ռ�����������Ӧ�Ӷ̹ܽ��룬��Ϊ�������ܶȱȿ���С����ѡc��
��4��ʵ������ȡCO2�����ڳ����£��ô���ʯ��ʯ��ʯ��ϡ������ȡ�ģ���ѧ����ʽΪ
![]() ��̼��ƺ����ụ�ཻ��Ӧ�������Ȼ��ƺ�ˮ�Ͷ�����̼����˲���Ҫ���ȣ�����װ�����ѡ��C��װ��C���ŵ��ǣ����Կ��Ʒ�Ӧ�ķ�����ֹͣ��
��̼��ƺ����ụ�ཻ��Ӧ�������Ȼ��ƺ�ˮ�Ͷ�����̼����˲���Ҫ���ȣ�����װ�����ѡ��C��װ��C���ŵ��ǣ����Կ��Ʒ�Ӧ�ķ�����ֹͣ��