题目内容
塑料袋的广泛使用,给我们的日常生活中带来了便利.常用的塑料袋有两种,一种是用聚乙烯[(C2H4)n]制成的,另一种是用聚氯乙烯[(C2H3Cl)n]制成的.某化学兴趣小组的同学收集了一种日常生活中常用的塑料袋,对其组成进行了如下探究:Ⅰ鉴别和分析
①取样,用坩埚钳夹持在酒精灯上燃烧,火焰呈黄色,且无刺鼻气味;由此可以初步确定该塑料袋是可能是由
②由于空气中氧气的体积分数为21%,因此用燃烧法确定塑料袋组成时,由于可能会生成既会产生污染,又会增加实验难度和实验误差的有毒气体
Ⅱ设计与实验
同学们设计了如图所示的装置,按下述步骤进行实验:
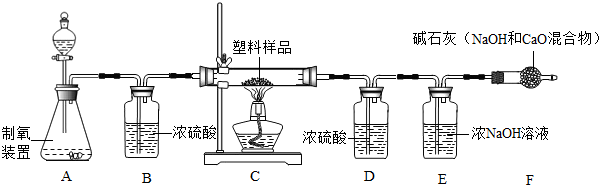
①连接好装置,检查气密性;②称取7.0g塑料样品,放入装置C中.称量D、E的质量;
③通入氧气一段时间后,加热塑料样品,使其燃烧;④塑料样品燃烧结束后,停止加热;
⑤继续通氧气至玻璃管冷却后,停止通氧气;⑥再次称量D、E的质量.
(3)思考与结论
①仪器F的作用是
②实验前将所用的塑料样品剪成碎屑的目的是
③将上述实验操作中的④、⑤颠倒可能导致的不良后果是
④若装置中没有连接仪器B,将使该塑料试样中氢元素的质量测算结果
⑤实验后发现D、E装置分别增重9.0g、22.0g,则该塑料中碳、氢元素质量比为
⑥塑料由于难以降解,造成白色污染.请说出生活中减少白色污染的一点措施:
分析:根据燃烧现象分出这两种塑料;含碳物质燃烧产生的有害气体主要是一氧化碳,得出第二个空的答案;然后分析题中实验装置,得出其它题的答案.
解答:答:用坩埚钳夹持在酒精灯上燃烧,火焰呈黄色,且无刺鼻气味;聚氯乙烯燃烧具有刺激性气味,聚乙烯燃烧不会产生刺激性气味,故(1)鉴别和分析的答案:①聚乙烯.
这两种塑料都是含碳化合物,含碳化合物燃烧产生的有毒气体是一氧化碳,故②答案:一氧化碳(或CO)
E中盛的是氢氧化钠溶液用于吸收二氧化碳,并通过测该装置增加的质量来推测塑料中碳氢元素质量比,F中装的是碱石灰同样可以吸水也与二氧化碳反应,并且空气中含有水蒸气和二氧化碳,故(3)思考与结论①答案:防止空气中的二氧化碳被E中的烧碱溶液吸收而影响碳元素含量的测定结果(或防止空气中的CO2进入E装置)
实验前将塑料撕碎之后它与酸的接触面积增大了,并且与酸的反应速度肯定加快,反应更充分.故②答案:增大塑料样品和氧气之间的接触面积,使反应充分;
若先停止通氧气C内氧气与塑料反应后C玻璃管内压强减小,小于外界大气压,液体会被从D内压入C,可这时玻璃管较热有可能炸裂,故③答案:液体会倒吸到玻璃管(烧管或平行管)中,导致其破裂(或D中液体倒流入C);
若不加B装置,制取氧气时的水蒸气会随之进入D,水比实际塑料燃烧产生的多.故④答案:偏大
D增加质量为水的质量,9g水中含有9g×
=1g;E增加的质量即塑料燃烧产生二氧化碳的质量,22g二氧化碳中碳的质量为22g×
=6g,故⑤答案:6:1.
白色污染是塑料制品造成的,只要想办法少造成塑料垃圾即可.故⑥答案:用布袋购物(其他合理答案均给分).
这两种塑料都是含碳化合物,含碳化合物燃烧产生的有毒气体是一氧化碳,故②答案:一氧化碳(或CO)
E中盛的是氢氧化钠溶液用于吸收二氧化碳,并通过测该装置增加的质量来推测塑料中碳氢元素质量比,F中装的是碱石灰同样可以吸水也与二氧化碳反应,并且空气中含有水蒸气和二氧化碳,故(3)思考与结论①答案:防止空气中的二氧化碳被E中的烧碱溶液吸收而影响碳元素含量的测定结果(或防止空气中的CO2进入E装置)
实验前将塑料撕碎之后它与酸的接触面积增大了,并且与酸的反应速度肯定加快,反应更充分.故②答案:增大塑料样品和氧气之间的接触面积,使反应充分;
若先停止通氧气C内氧气与塑料反应后C玻璃管内压强减小,小于外界大气压,液体会被从D内压入C,可这时玻璃管较热有可能炸裂,故③答案:液体会倒吸到玻璃管(烧管或平行管)中,导致其破裂(或D中液体倒流入C);
若不加B装置,制取氧气时的水蒸气会随之进入D,水比实际塑料燃烧产生的多.故④答案:偏大
D增加质量为水的质量,9g水中含有9g×
| 2 |
| 18 |
| 12 |
| 44 |
白色污染是塑料制品造成的,只要想办法少造成塑料垃圾即可.故⑥答案:用布袋购物(其他合理答案均给分).
点评:本题通过实验探究塑料的组成,考查了重点,思路清晰,各种能力综合考查,较为理想

练习册系列答案
相关题目
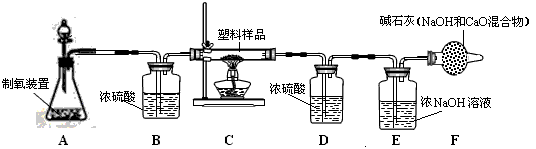

 我们的日常生活中带来了便利。常用的塑料袋有两种,一种是用聚乙烯[(C2H4)n]制成的,另一种是用聚氯乙烯[(C2H3Cl)n]制成的。某化学兴趣小组的同学收集了一种日常生活中常用的塑料袋,对其组成进行了如下探究:
我们的日常生活中带来了便利。常用的塑料袋有两种,一种是用聚乙烯[(C2H4)n]制成的,另一种是用聚氯乙烯[(C2H3Cl)n]制成的。某化学兴趣小组的同学收集了一种日常生活中常用的塑料袋,对其组成进行了如下探究:
 ⑥再次称量D、E的质量。
⑥再次称量D、E的质量。 色污染。
色污染。