题目内容
【题目】
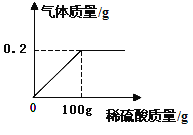
(1)该铁合金是生铁还是钢?
(2)加入的稀硫酸中溶质的质量分数?
(3)反应后所得溶液中溶质的质量分数?
【答案】(1)钢(2)9.8%(3)14.4%
【解析】试题分析:设样品中铁的质量为X,需要硫酸的量为Y,生成硫酸亚铁的质量为Z
Fe + H2SO4="=" Fe SO4+ H2↑
56 98 152 2
X Y Z 0.2克
列比例式得:56:X=98:Y=152:Z=2:0.2克解得:X=5.6克Y=9.8克Z=15.2克
样品中碳的质量分数为:(5.7g-5.6)÷5.7g×100%==1.8% < 2% 该铁合金是钢
加入的稀硫酸中溶质的质量分数:(9.8g÷100g)×100%==9.8%
反应后所得溶液中溶质的质量分数: 15.2g/(5.6g+100g-0.2g)]×100%==14.4%

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目