题目内容
【题目】将等质量的Mg、Al、 Fe分别放入三份浓度(即质量分数)相等的稀盐酸中,反应生成的氢气质量与反应时间的关系如图所示,根据图中所给信息,作出的判断错误的是( )
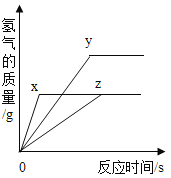
A.图线z表示铁的反应情况
B.铝消耗的稀盐酸质量最大
C.镁和铁一定有剩余,铝可能反应完
D.消耗铁的质量一定大于消耗镁的质量
【答案】C
【解析】
Mg、Al、Fe与稀盐酸反应时,物质之间的质量关系为:![]()
![]()
![]()
![]()
A. 根据转折点之前相等时间内产生氢气的质量可知,x金属活动性最强,x表示Mg,其次是y,y表示Al,z的金属活动性最弱,z表示铁的反应情况,此选项正确;
B. 由图可知,铝与稀盐酸反应生成的氢气最多,故铝消耗的稀盐酸质量最大,此选项正确;
C. 由图中信息可知,镁、铁与稀盐酸反应生成的氢气质量相等,说明镁一定过量,铁过量或恰好完全反应,如果镁过量,那么铝一定过量,镁、铝都过量时,生成的氢气质量应该相等,与图中信息不符,此选项错误;
D. 由图中信息可知,镁、铁与稀盐酸反应生成的氢气质量相等,故消耗铁的质量一定大于消耗镁的质量,此选项正确。
故选C。

练习册系列答案
相关题目
【题目】生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%~4.3%,钢中碳的含量为 0.03%~2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示:
烧杯质量 | 样品的质量 | 稀盐酸的质量 | 烧杯+剩余物的总质量 |
50g | 11.6g | 94.8g | 156g |
注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)生成氢气的质量为_____ g;
(2)样品中碳的质量分数_____ (计算结果保留到0.1%);
(3)反应后得到氯化亚铁质量_____。