题目内容
【题目】某校兴趣小组在实验室做测定一瓶稀硫酸浓度的实验,他们取出100克的稀硫酸,放入20克的金属锌,等到充分反应后,把剩余的锌烘干,称量共有7克。反应的化学方程式为:![]() 。请你根据以上的数据,帮助他们完成下列问题:
。请你根据以上的数据,帮助他们完成下列问题:
(1)硫酸中氢、硫、氧三种元素的质量比为_________(最简整数比)。
(2)硫酸中氧元素的质量分数为________%。(精确到0.1%)。
(3)这瓶稀硫酸中硫酸的质量分数是____________?(写出计算过程)
【答案】1:16:32 65.3 19.6%
【解析】
(1)硫酸中氢、硫、氧三种元素的质量比为(1×2):32:(16×4)=1:16:32;
(2)硫酸中氧元素的质量分数![]() ×100%≈65.3%;
×100%≈65.3%;
(3)由题意可得,参加反应锌的质量:20g-7g=13g,设100g稀硫酸中硫酸的质量为x,
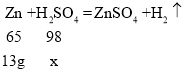
![]() ,
,
x=19.6g,
这瓶稀硫酸中硫酸的质量分数![]() 。
。

练习册系列答案
相关题目