题目内容
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:(1)P点的含义是
(2)t2℃时30g物质a加入到50g水中不断搅拌,形成溶液的质量是
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是
(4)在t2℃时,将等量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是
(5)当a中含有少量b时,可采用
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:(1)溶解度曲线的交点表示该温度下二者的溶解度相等;
(2)据该温度下a的溶解度分析解答;
(3)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(4)等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多,饱和溶液中溶解度小的溶质质量分数小.
(5)根据固体物质的溶解度受温度影响情况的大小分析结晶方法.
(2)据该温度下a的溶解度分析解答;
(3)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(4)等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多,饱和溶液中溶解度小的溶质质量分数小.
(5)根据固体物质的溶解度受温度影响情况的大小分析结晶方法.
解答:解:
(1)P点是t1℃时ac的溶解度曲线的交点,表示该温度下二者的溶解度相等;
(2)t2℃时a的溶解度是50g,即100g水中最多溶解50g的a,所以将30g的a加入到50g水中不断搅拌,最多溶解25g,形成75克溶液;
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是c<b<a;
(4)ab的溶解度随温度的降低而减小,所以降温会析出晶体,a的溶解度变化幅度较大,所以析出较多的是a;根据饱和时质量分数的计算式
×100%,即溶解度越大质量分数也就越大,t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温到t1℃,b的溶解度大于A的溶解度大于t2℃时C的溶解度,故所得溶液中溶质质量分数最小的是c;
(5)a的溶解度随温度升高而增大且受温度影响较大,若a中混有少量的b,获得纯净a的方法是冷却热饱和溶液结晶.
答案:
(1)t1℃时ac的溶解度相等;
(2)75;
(3)c<b<a;
(4)a c
(5)冷却热饱和溶液结晶
(1)P点是t1℃时ac的溶解度曲线的交点,表示该温度下二者的溶解度相等;
(2)t2℃时a的溶解度是50g,即100g水中最多溶解50g的a,所以将30g的a加入到50g水中不断搅拌,最多溶解25g,形成75克溶液;
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是c<b<a;
(4)ab的溶解度随温度的降低而减小,所以降温会析出晶体,a的溶解度变化幅度较大,所以析出较多的是a;根据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(5)a的溶解度随温度升高而增大且受温度影响较大,若a中混有少量的b,获得纯净a的方法是冷却热饱和溶液结晶.
答案:
(1)t1℃时ac的溶解度相等;
(2)75;
(3)c<b<a;
(4)a c
(5)冷却热饱和溶液结晶
点评:本题对于溶解度、溶解度曲线进行了考查,掌握相关知识才能结合题意灵活解答.

练习册系列答案
相关题目
下列符号既能表示一种元素,又能表示该元素的一个原子,还能表示一种物质的是( )
| A、O2 | B、3H |
| C、O | D、Fe |
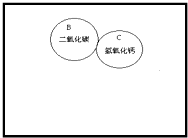 现有A(木炭)、B(二氧化碳)C(氢氧化钙溶液)、D(稀盐酸)、E(氧化铜)五种物质,两圆相切表示两种物质可以发生反应,回答下列问题
现有A(木炭)、B(二氧化碳)C(氢氧化钙溶液)、D(稀盐酸)、E(氧化铜)五种物质,两圆相切表示两种物质可以发生反应,回答下列问题 表示氯原子,
表示氯原子, 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)
 (1)用“
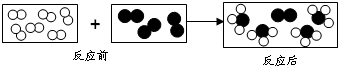
(1)用“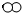 ”和“
”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:写出上述过程发生的化学反应的方程式:
”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:写出上述过程发生的化学反应的方程式: