题目内容
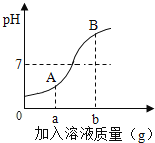
【题目】小华同学走进实验室看到一瓶蓝色的溶液很感兴趣,实验老师告诉他这瓶蓝色的溶液是硫酸与硫酸铜的混合溶液。于是他在实验老师的指导下进行探究。他取26.8g该废液于小烧杯中,然后滴加10%的氢氧化钠溶液,并绘了如下图所示的坐标图:请根据图像计算:

(1)生成沉淀a是多少克?
(2)反应后所得溶液中溶质的质量分数是多少?
【答案】(1)1.96g(2)10%
【解析】
(1)由图可知生成沉淀消耗氢氧化钠溶液16g设生成氢氧化铜沉淀质量为x,硫酸钠质量为y。
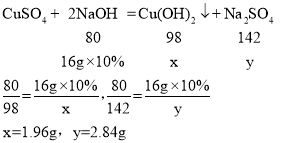
故填:1.96g
(2)解:由图可知和硫酸反应的氢氧化钠溶液质量16g,设生成硫酸钠质量为z。
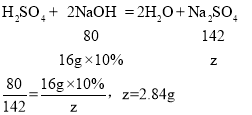
硫酸钠质量:2.84g+2.84g=5.68g
溶液质量:26.8g+32g-1.96g=56.84g
溶质质量分数:
![]()
答:溶质质量分数10%

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
【题目】(4分)合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要。
(1)2013年12月广州建业大厦发生严重火灾。从燃烧条件分析,大厦内存放的大量鞋、纸箱等物品充当了________________。
(2)高层建筑物通常设计了灭火用的洒水系统。从灭火原理分析,洒水的作用主要是______________。
(3)分析下表中的数据,回答问题:
物质代号 | L | M | N | P |
熔点/℃ | -117 | 3550 | 44 | -259 |
沸点/℃ | 78 | 4827 | 257 | -253 |
着火点/℃ | 510 | 370 | 40 | 580 |
①有人认为“物质的熔、沸点越高,着火点越高”,该结论_______________(填“合理”或“不合理”)。

②已知酒精灯火焰的温度约为500℃。利用上图装置,验证达到可燃物着火点是燃烧的条件之一,上表中可用于完成该实验的两种可燃物是_________和________(填代号)。