题目内容
【题目】某化学兴趣小组同学利用图中所示装置模拟炼铁:
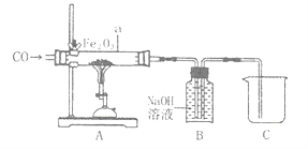
(1)为了避免玻璃管a在加热时可能发生爆炸,加热前应 。
(2)a管中氧化铁发生反应的化学方程式为 。
(3)B装置可用来吸收二氧化碳气体,写出该反应的化学方程式 ;B装置 (填“能”或“不能”)用来收集CO。
(4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中氧化铁的质量是 g。
【答案】(1)先通一会儿CO (2)3CO+Fe2O3高温2Fe+3CO2
(3)CO2+2NaOH=Na2CO3+H2O 能 (4)8
【解析】
试题分析:(1)CO具有可燃性,当CO与空气混合时,在点燃时可能发生爆炸,故为了避免玻璃管a在加热时可能发生爆炸,加热前应先通一会儿CO,将玻璃管内的空气排净
(2)CO还原氧化铁反应的化学方程式为:3CO+Fe2O3高温2Fe+3CO2
(3)B装置中盛放的是NaOH溶液,可用来吸收二氧化碳气体,发生反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;由于CO不能与NaOH溶液反应,故B装置能用来收集CO
(4)根据化学方程式:3CO+Fe2O3高温2Fe+3CO2分析,a管反应前后质量差,实际就是Fe2O3中氧元素的质量,再根据元素质量=物质质量×元素质量分数,故可设氧化铁质量为x,列式为:2.4g =x×48/160×100%,所以x=8g

练习册系列答案
相关题目