题目内容
【题目】有一种淡黄色粉末可制备消毒杀菌剂。兴趣小组对其成分进行了探究。
(提出问题)淡黄色固体是什么?
(查阅资料)(1)硫粉是一种淡黄色固体,难溶于水,燃烧生成刺激性气味的有毒气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应放出气体。
(设计实验)
方案一:取少量该固体粉末于试管中,加5mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
经过讨论,兴趣小组决定采用方案一,其理由是_____(选填字母)。
A.操作简单 B.无实验污染 C.节约能源
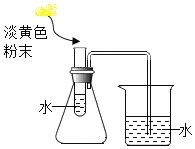
(实验验证)用如图装置实验,将淡黄色粉末加入试管中
①若无现象,则此粉末为_____,
②若淡黄色粉末为过氧化钠,可观察到试管中的现象是_____,烧杯中出现气泡,说明_____。
(实验结论)实验确定该淡黄色粉末是过氧化钠。
(问题讨论)兴趣小组通过讨论,认为过氧化钠(Na2O2)与水反应生成O2.你可采用_____操作加以验证。
【答案】ABC;硫粉;产生气泡;过氧化钠与水反应放热;将带火星木条伸入试管;
【解析】
硫粉燃烧生成刺激性气味的有毒气体,污染空气,利用过氧化钠(Na2O2)能与水反应放出气体,操作简单,节约能源,不污染空气;硫不与水反应,所以若无现象,则此粉末为硫磺;若淡黄色粉末为过氧化钠,则会生成气体,可观察到试管中的现象是有气泡产生,同时烧杯中出现气泡,说明反应中放出热量,使锥形瓶内气体受热膨胀逸出;过氧化钠(Na2O2)与水反应生成氢氧化钠(NaOH)和一种单质气体,由质量守恒定律,反应前后元素的种类不变,可推出气体为氧气。
(1)经过讨论,兴趣小组决定采用方案一,其理由是操作简单,无实验污染,节约能源。故选ABC;
(2)用如图装置实验,将淡黄色粉末加入试管中,①若无现象,则此粉末为硫粉;
②若淡黄色粉末为过氧化钠,则过氧化钠和水反应生成氧气,可观察到试管中产生气泡;如果过氧化钠与水反应放热,会导致锥形瓶中的气体压强增大,从而导致烧杯中出现气泡;
(3)兴趣小组通过讨论,认为过氧化钠(Na2O2)与水反应生成O2,可以将带火星木条伸入试管加以验证,如果带火星的木条复燃,说明反应生成氧气,反之不产生氧气。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】下列实验指定容器中的水,其解释没有体现水的主要作用的是![]()
![]()
A | B | C | D | |
实 验 装 置 |
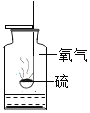
硫在氧气中燃烧 |
测定空气中氧气含量 |
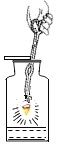
铁丝在氧气中燃烧 |
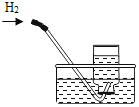
排水法收集氢气
|
解释 | 集气瓶中的水:吸收放出的热量和二氧化硫 | 量筒中的水:通过水体积的变化得出 | 集气瓶中的水:吸收有害物质,防止大气污染 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察氢气何时收集满 |
A. A B. B C. C D. D