题目内容
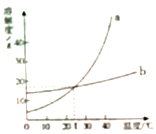
【题目】如图是 A、B 两物质的溶解度曲线,下列信息中正确的是

A. 图中阴影部分表明 A、B 两溶液都是饱和溶液
B. t1℃时,A、B 两饱和溶液的溶质质量分数相等
C. t2℃时,B 物质的溶解度大于 A 物质的溶解度
D. t2℃时,等质量的 A、B 两饱和溶液降温到 t1℃时析出溶质的质量相等
【答案】B
【解析】
A、图中阴影部分表明A溶液是饱和溶液,B溶液是不饱和溶液,故A错误;B、t1℃时,A、B物质的溶解度相等,所以饱和溶液的溶质质量分数相等,故B正确;C、通过分析溶解度曲线可知,t2℃时,B物质的溶解度小于A物质的溶解度,故C错误;D、t2℃时,A物质的溶解度大于B物质的溶解度,t1℃时,A、B物质的溶解度相等,所以等质量的A、B两饱和溶液降温到t1℃时析出溶质的质量A大于B,故D错误。故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组利用稀盐酸和澄清石灰水展开“酸碱中和反应”的实验探究活动。请你参与他们的实验活动,并回答相关问题
(提出问题Ⅰ)稀盐酸和澄清石灰水能否发生反应?
(实验1)小明取一定量的稀盐酸,测得其pH=2,然后向其中加入一定量的澄清石灰水后,测得混合溶液的pH=3,于是得出“稀盐酸和澄清石灰水发生了中和反应”的结论。
测定溶液pH的方法是:将pH试纸放在玻璃片上,___,将试纸显示的颜色与标准比色卡比较。
小刚认为,小明的实验方案不能证明二者发生了中和反应,理由是___。
(实验2)小刚取稀盐酸于试管中,加入一定量的澄清石灰水,得到溶液X,再加入适量铁粉,观察到___,证明稀盐酸和澄清石灰水发生了反应。
稀盐酸和澄清石灰水反应的化学方程式为___。
(提出问题Ⅱ)溶液X中溶质的成分是什么?
猜想一:只有CaCl2;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和HCl
小组同学为验证猜想二,进行了如下实验(查阅资料显示CaCl2溶液显中性)
实验操作 | 实验现象 | 实验结论 | |
实验3 | 取适量溶液X于试管中,滴加紫色石蕊溶液 | ___ | 猜想二成立 |
实验4 | 取适量溶液X于试管中,滴加Na2CO3溶液 | 产生白色沉淀 | 猜想二成立 |
小明认为实验4中产生白色沉淀,并不能证明猜想二成立,理由是____。
请你另选一种试剂,设计合理的方案,当观察到与实验4相同的现象时,证明猜想二成立。你的实验原理是___(用化学方程式表示)。
【题目】小明在课外阅读中得知:氢氧化铜受热会分解生成氧化铜(Cu(OH)2![]() CuO+X),于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
CuO+X),于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)生成物X的化学式为____。
(2)小明在加热氢氧化铜时,发现蓝色固体先变成黑色,继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成分,进行了如下的探究:
(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu;Ⅱ.Cu2O;Ⅲ. ____。
(进行实验)
操作 | 现象 | 结论 |
①取灼烧后的红色固体1.44 g于试管中,加入足量稀硫酸,加热并充分振荡,静置 | 溶液由无色变蓝色,固体减少 | 1.44 g红色固体一定有__ |
②过滤、洗涤、干燥 | 得红色固体 |
(结论分析)
①根据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想__也有相同现象。
②氧化铜高温灼烧由黑色变成红色的化学反应方程式为____。
③如要确定1.44 g红色固体成分,还需要补充的操作是__,再通过____得出结论。