题目内容
【题目】从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如图所示。

(1)X的化学式为______,该反应类型是_____(填基本反应类型)。
(2)反应前后硅元素的化合价_____(填“升高”或“降低”)。
【答案】HCl 置换反应 降低
【解析】
(1)根据反应前后原子种类、数目均不变。反应前共有Si、H、Cl三种原子个数依次为1、4、4,反应后Si原子1个、故4X含有H、Cl个数依次为4、4,故X的化学式为HCl;该反应的化学方程式为: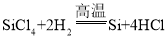 ,该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;故填:HCl,置换反应。
,该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;故填:HCl,置换反应。
(2)在反应物四氯化硅中硅的化合价为+4价,生成物单质硅中化合价为0价,反应前后硅元素的化合价降低。故填:降低

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
试计算:
(1)完全反应后生成二氧化碳的质量为____________g;
(2)求该珍珠粉中碳酸钙的质量分数为____________。