题目内容
【题目】定量研究对于化学的发展有重大作用。
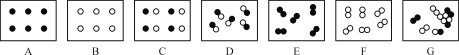
(1)图A、B、C所示实验中,反应前后的称量结果会有变化的是_____(填字母)。

(2)图A锥形瓶中发生反应的化学方程式为_________。书写化学方程式要遵守两个原则:一是________,二是要遵守质量守恒定律。
(3)化学反应前后肯定没有变化的是______(填字母)。
A.元素种类 B.原子种类 C.原子数目 D.原子质量
【答案】B 4P+5O2 ![]() 2P2O5 要以客观事实为基础 ABCD
2P2O5 要以客观事实为基础 ABCD
【解析】
(1)A、红磷燃烧生成五氧化二磷固体,且该装置由气球进行密封,故反应前后没有质量变化;B、碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体,且装置敞口,故二氧化碳气体会逸出,反应前后质量发生变化;C、铁和硫酸铜溶液反应生成铜和硫酸亚铁,反应物和生成物均没有气体,故反应前后质量不变。故本题选B。
(2)红磷燃烧生成五氧化二磷固体,反应的化学方程式为4P+5O2 ![]() 2P2O5;书写化学方程式要遵守两个原则:一是要以客观事实为基础,二是要遵守质量守恒定律;
2P2O5;书写化学方程式要遵守两个原则:一是要以客观事实为基础,二是要遵守质量守恒定律;
(3)化学反应前后肯定没有变化的是元素种类、原子种类、原子数目、原子质量。故本题选ABCD。

 名校课堂系列答案
名校课堂系列答案【题目】空气中氧气含量测定的再认识
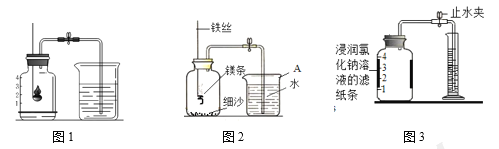
Ⅰ. 用红磷测定空气中氧气的含量。
(1)请写出红磷在空气中燃烧的化学表达式________。
(2)如图1所示进行实验, 测得空气中氧气的含量小于1∕5,可能的原因是 ____(填序号)。
A.燃烧匙伸入集气瓶太慢 B.红磷量不足
C. 实验中发现导管口有气泡冒出 D.装置漏气
Ⅱ. 用镁条测定空气中氧气的含量。
(3)请写出镁条在氧气中燃烧的化学表达式_____________。
(4)某同学利用图2实验测定空气中氧气含量时发现,产物中还出现少许黄色固体。
已知:镁能与氮气反应生成淡黄色的氮化镁(Mg3N2)固体。 但在空气中燃烧镁条时很难观察到生成物中有淡黄色固体,原因是_________。在操作规范的情况下,该同学实验所测得的氧气体积分数______1/5(填“大于”、“小于”或“等于”)。
Ⅲ. 用铁粉测定空气中氧气的含量。
(5)已知铁常温下与空气中的氧气、水反应生成铁锈(主要成分是Fe2O3﹒xH2O)。试写出该反应的化学表达式________。
(6)某同学根据铁生锈的原理,用铁粉测定空气中氧气的含量,设计了如图实验,8分钟后测得数据如表:
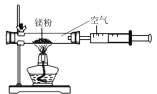
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 量筒内水 | 量筒内剩余水 |
250mL | 180.0mL | 129.5mL |
实验时该同学不是将铁粉堆在瓶底,而是将铁粉撒在浸润了氯化钠溶液的滤纸条上,再把该滤纸条贴在广口瓶内侧,其目的是________。根据表中数据计算得出空气中氧气的体积分数为________(结果保留到0.1%)。与用红磷燃烧的方法相比,用该方法测定空气中氧气的含量的主要优点一是没有污染,二是 ____________。
Ⅳ.拓展应用
(7)取2.4g镁条在O2和N2的混合气体中完全燃烧,所得固体质量为ag,,则a的取值范围是________g<a g<4g(结果保留到0. 1g)。
(8)已知:Fe2O3固体在一定的高温下能分解为一种复杂的铁的氧化物和一种气体。 该气体可以用___________来检验。现将64.0gFe2O3固体加热到该温度下,发现固体质量减少了3.2g后质量不再改变。请回答:64.0gFe2O3固体中含有铁元素_______g;该温度下复杂的铁的氧化物的化学式为__________。
【题目】完成下列实验题
(实验一)结合净化黄泥水的活动经验和加工自来水的原理,指出下列杂质的除去方法(填方法名称)
水中杂质种类 | 除去杂质的方法名称 |
颗粒较大的不溶性杂质 | ____ |
颗粒较小的不溶性杂质 | ____ |
可溶性杂质 | ____ |
(实验二)实验室欲配制一定质量分数的食盐溶液。请完成下列问题:
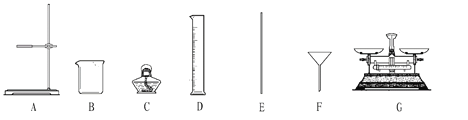
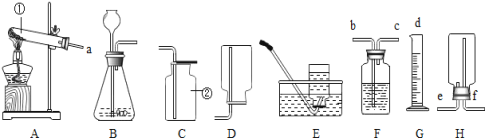
(1)B仪器的名称是_______,D仪器的名称是_____。
(2)完成本实验,所需仪器除B、E外,还必须选用上述仪器中的_______(填仪器编号),仪器E的作用是_______。
(3)配制的步骤可以概括为计算、称量和量取、_______、装瓶。
(4)如果量取水的体积时,操作者的视线是仰视,则所配溶液的质量分数将_______(填“偏大”或“偏小”或“不变”)。