题目内容
(7 分)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。某化学研究小组的同学欲对某种塑料袋的组成进行分析研究,测定样品中元素的质量比,设计了如图所示的实验装置。
(小资料:该种塑料袋只含碳、氢两种元素,燃烧产物为二氧化碳和水。图中碱石灰可以吸收空气中的二氧化碳与水蒸气)
(1)按上面连接好装置,在装入药品之前,必须进行的操作是 。
(2)装置 A 中所发生的反应化学方程式为 。装置中 MnO2 粉末的作用是 。
(3)由于发生装置 A 制取的氧气中混有水蒸气,为不影响测定结果,装置B中盛放的试剂应该是_____________(写名称)。
(4)判断塑料袋试样中含有碳元素的依据是____________________________________。
(5)根据实验前后装置的质量变化测算出仪器D质量增重5.4g,仪器 E 质量增重 8.8g,则该塑料袋试样中碳元素与氢元素的质量比为______________。
(6)若实验过程中由于过氧化氢的量不足,塑料袋试样燃烧不充分,则该塑料试样中碳 元素与氢元素的质量比的测算结果 (填“一定偏大”、“一定偏小”、“基本一致”之一)。
(1)检查装置的气密性(2)2H2O2MnO22H2O+O2↑;催化作用(3)浓硫酸(4)E装置中澄清石灰水变浑浊(5)4∶1;(6)基本一致
解析试题分析:(1)按上面连接好装置,在装入药品之前,必须进行的操作是检查装置的气密性;(2)装置 A 中所发生的反应化学方程式为2H2O2MnO22H2O+O2↑,装置中 MnO2 粉末的作用是催化作用;(3)由于发生装置 A 制取的氧气中混有水蒸气,为不影响测定结果,装置B中盛放的试剂应该是具有吸水性的浓硫酸;(4)判断塑料袋试样中含有碳元素的依据是生成二氧化碳,故E装置中澄清石灰水变浑浊;(5)根据实验前后装置的质量变化测算出仪器D质量增重5.4g,仪器 E 质量增重 8.8g,则该塑料袋试样中碳元素与氢元素的质量比为:8.8g×12/44 :5.4g×2/18= 2.4g:0.6g="4:1;" (6)若实验过程中由于过氧化氢的量不足,塑料袋试样燃烧不充分,则该塑料试样中碳 元素与氢元素的质量比的测算结果基本一致。
考点:物质成分的的探究

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案化学实验室有一盖玻璃片的集气瓶,正放在桌面上,不知盛有何种气体?请你作出一种假说(猜想),并按你的假设填表,完成探究过程。
| 假设(猜想) | 验证方法及操作 | 可能看到的现象 | 结论 |
| | | | |
(5分)实验创新是中学生最为重要的科学素养.下图是某学校师生对“MnO2催化H2O2分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为lg/ml)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2gMnO2粉末,加在干燥的进气管的管壁上。
②点燃橡胶塞上固定的棒香后,塞紧干燥管并将其竖立,观察现象。
请分析回答:
(1)可观察带到火星的棒香立即 。
(2)写出上述实验发生的化学反应方程式 。
(3)下列各项是同学们对该创新实验的评价,你认为评价不合理的是 。(填序号)
| A.实验中所用的仪器、材料及药品均易得到 |
| B.实验使用的药品用量太大 |
| C.反应速度太慢,耽误时间 |
| D.实验现象明显,整个装置好似点燃的灯塔,趣味性强 |





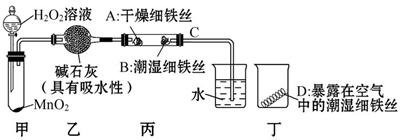

 CO↑+H2O。实验室可利用下图装置制取CO并还原CuO。请回答下列问题:
CO↑+H2O。实验室可利用下图装置制取CO并还原CuO。请回答下列问题: