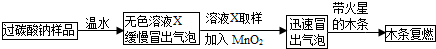题目内容
同学们在学习化学的过程中有下列说法或做法,你认为正确的是( )
| A、Al2O3读作“氧化铝” | ||||
| B、五氧化二磷的化学式写成“O5P2” | ||||
C、2H2+O2
| ||||
| D、尿素[CO(NH2)2]相对分子质量的计算式写成“12+16+14+1×2×2=46” |
分析:A、化合物化学式的读法:一般是从右向左读,读作“某化某”,有时还要把元素符号右下角的数字读出来,如SO2、P2O5等,据此进行分析判断.
B、化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
C、读化学方程式时,“+”应读作“和”,“═”应读作“生成”.
D、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
B、化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
C、读化学方程式时,“+”应读作“和”,“═”应读作“生成”.
D、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
解答:解:A、Al2O3从右向左读,读作氧化铝,故选项说法正确.
B、五氧化二磷的化学式为P2O5,故选项说法错误.
C、在反应中“+”读作“和”,“═”读应作“生成”,该反应可读作:氢气和氧气在点燃条件下生成水,故选项说法错误.
D、尿素[CO(NH2)2]相对分子质量为12+16+(14+1×2)×2,故选项说法错误.
故选:A.
B、五氧化二磷的化学式为P2O5,故选项说法错误.
C、在反应中“+”读作“和”,“═”读应作“生成”,该反应可读作:氢气和氧气在点燃条件下生成水,故选项说法错误.
D、尿素[CO(NH2)2]相对分子质量为12+16+(14+1×2)×2,故选项说法错误.
故选:A.
点评:本题难度不大,掌握化合物化学式的书写方法与读法、化学方程式的含义、化学式的有关计算等即可正确解答本题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
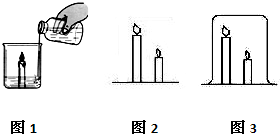 24、在高效课堂中,老师和同学们一起对“灭火的原理”进行了探究学习.
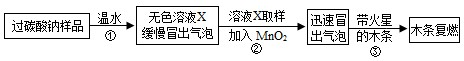
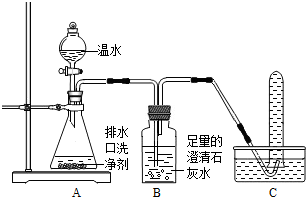
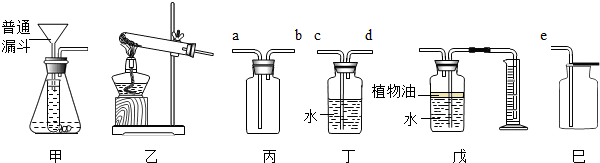
24、在高效课堂中,老师和同学们一起对“灭火的原理”进行了探究学习.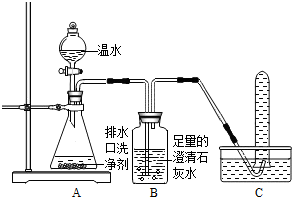 (2013?潍城区二模)小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.
(2013?潍城区二模)小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.