题目内容
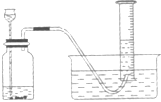
【题目】为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图),他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如下表:
反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
(1)由实验结果可知:金属活动性较强的是 .
(2)为了使得到的实验数据准确,小吴开始收集气体的时间点应该是 .
A.导管口一有气泡冒出时 B.冒出气泡连续且均匀时 C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道 .
A.参加反应的硫酸质量 B.生成物中金属元素的化合价.
【答案】(1)乙;(2)A;(3)B.
【解析】
试题分析:根据表格数据可知相同时间内金属乙产生的气体比甲多,因此乙的活动性比甲强;(2)因为要测定金属产生氢气的快慢,因此应该是收集金属反应产生的所有气体,故是导管口一有气泡冒出时就要收集,故选项为:A;(3)已知金属的质量、产生氢气的质量,根据化学方程式进行计算金属的相对原子质量,因此缺少金属的化合价来书写化学方程式,故选项为:B;

练习册系列答案
相关题目