题目内容
【题目】下面是用红磷或白磷进行的几个实验,请根据要求回答问题:
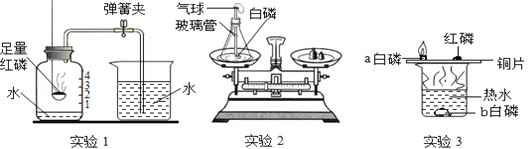
(1)实验1是利用红磷消耗瓶内的_______,使瓶内压强减少来推测空气里氧气的含量;写出红磷燃烧的化学方程式是__________________。
(2)实验2的目的是验证质量守恒定律。操作时先将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,反应后,冷却,再称量装置总质量,发现托盘天平保持平衡。整个实验过程中气球会出现的现象是(填字母)_______。 A.先膨胀后缩小 B.持续膨胀 C.无变化
(3)实验3的目的是探究可燃物燃烧的条件,仅由a处白磷燃烧,铜片上红磷没有燃烧这一现象,可得到的结论是:可燃物燃烧的条件之一是___________________________。
【答案】 O2 4P+ 5O2点燃2P2O5 A 温度达到可燃物的着火点
【解析】(1)实验1是探究空气中氧气的体积含量;红磷在空气中燃烧生成五氧化二磷,故化学方程式是: 4P+ 5O2![]() 2P2O5 ;(2)根据锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷熄消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;(3)白磷具有可燃性,温度也都达到了白磷的着火点,a处的白磷与氧气接触而发生燃烧,铜片上红磷没有燃烧这一现象,故可得出的结论是:可燃物燃烧时温度达到可燃物的着火点。
2P2O5 ;(2)根据锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷熄消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;(3)白磷具有可燃性,温度也都达到了白磷的着火点,a处的白磷与氧气接触而发生燃烧,铜片上红磷没有燃烧这一现象,故可得出的结论是:可燃物燃烧时温度达到可燃物的着火点。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目