题目内容
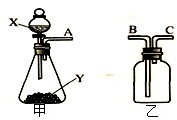 如图是实验室常用的两个气体制备、收集、净化的多种功能装置.
如图是实验室常用的两个气体制备、收集、净化的多种功能装置.(1)装置甲下面部位仪器的名称是
锥形瓶
锥形瓶
;(2)若制备的气体是氢气,且产生的气体中不含酸性杂质气体,则试剂X常用
稀硫酸
稀硫酸
,用装置乙收集氢气时,瓶口向上,则甲、乙两装置,其导管连接位置应是A接C
C
(选填B或C);(3)若X是稀盐酸、Y是石灰石,用甲、乙两装置组成发生、净化、收集CO2气体的系列装置.若乙中放入饱和NaHCO3溶液,该溶液的作用是除去
氯化氢杂质
氯化氢杂质
;发生的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
,若乙中放入浓硫酸,浓硫酸的作用是吸水干燥
吸水干燥
.分析:(1)熟练掌握常见化学仪器的名称及其用途;
(2)根据金属和盐酸或稀硫酸反应产生氢气分析;根据氢气的密度选择进气口;
(3)根据实验的目的、要求分析碳酸氢钠的作用;稀盐酸与石灰石反应制取二氧化碳,根据碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;结合实验的目的和浓硫酸的作用分析.
(2)根据金属和盐酸或稀硫酸反应产生氢气分析;根据氢气的密度选择进气口;
(3)根据实验的目的、要求分析碳酸氢钠的作用;稀盐酸与石灰石反应制取二氧化碳,根据碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;结合实验的目的和浓硫酸的作用分析.
解答:解:(1)装置甲下面部位仪器的名称是锥形瓶,可以用作反应容器;
(2)制备氢气可以是锌和稀盐酸或稀硫酸反应,要求产生的气体中不含酸性杂质气体,因为盐酸具有挥发性,故不能用稀盐酸,所以试剂X常用稀硫酸;因为氢气的密度比空气小,故通过短管C进入,把空气从长管排出;
(3)因为稀盐酸和石灰石反应时,因为盐酸的挥发性会使二氧化碳中混有氯化氢杂质,NaHCO3溶液能够和氯化氢反应产生二氧化碳,因此饱和NaHCO3溶液的作用是除去氯化氢杂质;
碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸具有吸水性,可以除去二氧化碳中的水蒸气得到干燥的二氧化碳.
故答案为:(1)锥形瓶;(2)稀硫酸;C;(3)氯化氢杂质;(4)CaCO3+2HCl=CaCl2+H2O+CO2↑;吸水干燥.
(2)制备氢气可以是锌和稀盐酸或稀硫酸反应,要求产生的气体中不含酸性杂质气体,因为盐酸具有挥发性,故不能用稀盐酸,所以试剂X常用稀硫酸;因为氢气的密度比空气小,故通过短管C进入,把空气从长管排出;
(3)因为稀盐酸和石灰石反应时,因为盐酸的挥发性会使二氧化碳中混有氯化氢杂质,NaHCO3溶液能够和氯化氢反应产生二氧化碳,因此饱和NaHCO3溶液的作用是除去氯化氢杂质;
碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸具有吸水性,可以除去二氧化碳中的水蒸气得到干燥的二氧化碳.
故答案为:(1)锥形瓶;(2)稀硫酸;C;(3)氯化氢杂质;(4)CaCO3+2HCl=CaCl2+H2O+CO2↑;吸水干燥.
点评:本题考查了实验室制气体的原理以及气体的干燥和除杂,综合性比较强.本题型要充分利用题目给出的信息,完成相关的问题.

练习册系列答案
相关题目
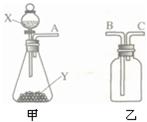 33、如图是实验室常用的两个气体制备、收集、净化的多种功能装置.
33、如图是实验室常用的两个气体制备、收集、净化的多种功能装置. 如图是实验室常用的两个气体制备、收集、净化的多种功能装置.
如图是实验室常用的两个气体制备、收集、净化的多种功能装置.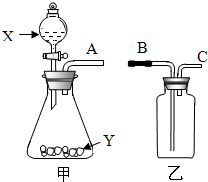 (2012?德城区二模)如图是实验室常用的两个气体制备、收集、净化的多功能装置.
(2012?德城区二模)如图是实验室常用的两个气体制备、收集、净化的多功能装置.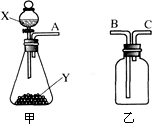 如图是实验室常用的两种气体制备、收集、净化的多种功能装置.请完成下列各题.
如图是实验室常用的两种气体制备、收集、净化的多种功能装置.请完成下列各题.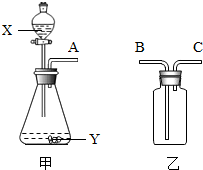 (2012?孝南区模拟)如图是实验室常用的两个气体制备、收集、净化的多种功能装置.
(2012?孝南区模拟)如图是实验室常用的两个气体制备、收集、净化的多种功能装置.