题目内容
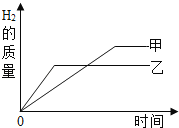
【题目】把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余.产生H2的质量随时间变化的趋势如图.下列说法中正确的是( )
A.甲的活动性比乙强
B.甲的相对原子质量一定比乙小
C.反应消耗等质量的硫酸
D.反应消耗等质量的金属
【答案】D
【解析】A、反应完全时乙用的时间少,反应速度快,活动性较强,即乙的活动性比甲强,故A说法错误;
B、根据金属与酸反应时,一定量金属完全反应产生氢气质量=![]() ×金属的质量,所以甲的相对原子质量不一定比乙小,如铝和镁,故B说法错误;
×金属的质量,所以甲的相对原子质量不一定比乙小,如铝和镁,故B说法错误;
C、生成氢气量的不同,说明消耗酸的质量不同,因为氢气来源于酸中的氢,故C说法错误;
D、放入的金属质量相等,反应后均无剩余,所以反应消耗等质量的金属,故D说法正确.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】石灰石是我市主要矿产之一,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验.
实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
实验图示 |
| |||
实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)