题目内容
【题目】原子结构与元素的性质和物质的组成密切相关,请将答案填写在下面的横线上:
(1)镁原子的结构示意图为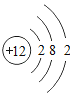 ,其在化学反应中易___________(填“得到”或“失去”)电子,其离子符号是____________ 。
,其在化学反应中易___________(填“得到”或“失去”)电子,其离子符号是____________ 。
(2)钠元素与氯元素组成的化合物是__________(化学式),构成该物质的微粒是__________(选填“分子”、“原子”、或“离子”)。
(3)与元素化学性质关系最密切的是____________(填字母编号)。
A元素的相对原子质量
B元素的核电荷数
C原子的核外电子数
D原子的最外层电子数
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是__________(填字母编号)。
A构成它们的原子大小不同
B构成它们的原子数目不同
C金刚石、石墨由不同种原子组成
D金刚石、石墨里碳原子排列方式不同
(5)铅元素相关信息如图所示。下列说法中正确的是___________。
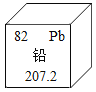
A铅原子核内有82个质子
B相对原于质量为207.2 g
C铝有毒,儿童不能使用铅笔
D铅不能与稀硫酸反应,产生氢气
【答案】失去 Mg2+ NaCl 离子 D D A
【解析】
(1)镁原子核外有2个电子其在化学反应中易失去2个电子带2个单位正电荷,其离子符号是:Mg2+;
(2)钠元素与氯元素组成的化合物是氯化钠:NaCl,该物质是由钠离子和氯离子构成的,构成该物质的微粒是离子。
(3)与元素化学性质关系最密切的是:原子最外层电子数;
故选:D。
(4)金刚石、石墨都是由碳元素组成,它们的化学性质相似,物理性质却有很大差异。其原因是:金刚石、石墨里碳原子排列方式不同;
故选:D。
(5)铅元素相关信息如图所示。下列说法中正确的是:
A、铅原子核内质子数=原子序数=82;故选项正确;
B、相对原于质量为207.2 ,单位不是“g”;故选项错误;
C、铝有毒,但铅笔中的铅不是以单质形式存在,儿童可以使用铅笔;故选项错误;
D、铅的金属活动顺序在氢前面,铅能与稀硫酸反应,产生氢气;故选项错误;
故选:A。

【题目】理科实验操作考试中,小明同学在做铝和稀盐酸反应时无意中加入硫酸铜溶液,发现铝片表面上产生气泡速率明显增快,对此他产生了兴趣。
(提出问题)硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
(设计实验1)室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10﹪稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率。
实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
硫酸铜饱和溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(1)上述表格中V=__________。
(2)写出铝和稀盐酸反应的化学方程式__________。
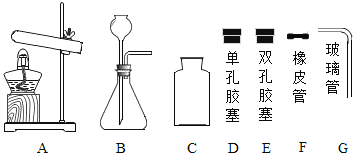
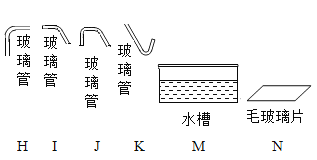
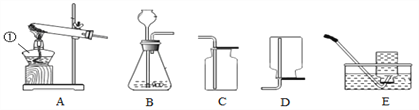
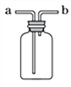
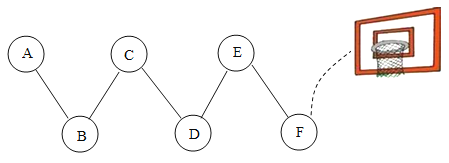
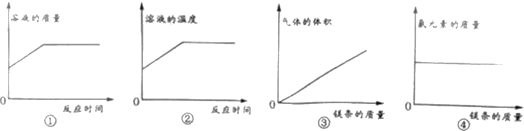
(3)定量收集氢气体积可用如图__________(填字母序号)装置。
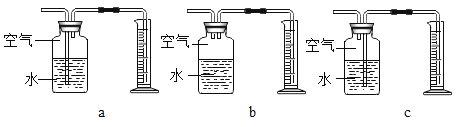
(实验现象)随着硫酸铜溶液体积的增加,产生氢气的速率先快后慢,且铝片表面附着的红色物质逐渐增加。
(结论与解释)
(4)随着硫酸铜溶液体积的增加,反应速率明显变慢可能的原因是_______________。
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是______________。
(实验反思)加快铝和稀盐酸反应速率还可以采取的措施是(写一点)_____________。
(设计实验2)根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10﹪稀盐酸混合后加入不同的盐溶液,实验现象如下(加号越多,代表反应速率越快)。
实验 | ① | ② | ③ | ④ | ⑤ |
加入试剂0.5mL | 水 | 5﹪NaCl溶液 | 5﹪Mg(NO3)2溶液 | 5﹪FeSO4溶液 | 5﹪CuSO4溶液 |
产生气泡速率 | + | + | + | ++ | +++ |
(6)上表中,用水进行实验的目的是_______________。
(7)上述实验设计存在有缺陷,该缺陷是_____________。改进实验后,仍符合上表中的实验现象,可得到的实验结论是_________(写一点)。