题目内容
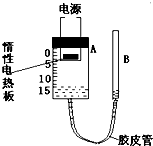 某研究性学习小组设计了如图所示的装置,探究空气中氧气的体积分数(已知:铜和氧气在加热条件下生成氧化铜),其中A是底面积50cm、高20cm的园筒状玻璃容器(带密封盖),上面标有以cm为单位的刻度,B是带刻度的敞口玻璃管(其他辅助装置略).
某研究性学习小组设计了如图所示的装置,探究空气中氧气的体积分数(已知:铜和氧气在加热条件下生成氧化铜),其中A是底面积50cm、高20cm的园筒状玻璃容器(带密封盖),上面标有以cm为单位的刻度,B是带刻度的敞口玻璃管(其他辅助装置略).
他们的操作过程如下:
a.检查装置的气密性;
b.加水并调整B的高度,使A中的液面至刻度15cm处;
c.将过量的铜粉平铺在惰性电热板上,盖好密封盖.
d.通电加热铜粉,待反应充分后,冷却到原来的状况,调整B的高度使A、B容器的液面保持水平,记录液面刻度.(注:A容器内固态物质所占的体积忽略不记)
(1)在上述实验中,下列物质能代替铜粉的是________(填序号)
A.红磷 B.木炭 C.铁粉 D.硫
(2)在操作d结束时,装置A中液面约为________cm(填整数).如果在操作结束时,装置A中液面刻度在13cm处,则实验结果比理论值________(填“偏大”或“偏小”).
解:(1)木炭和硫分别与氧气反应生成二氧化碳和二氧化硫气体,所以不能代替铜粉做实验,而铁与空气中氧气反应很慢,所以不可以代替铜粉,而红磷与空气中氧气反应生成五氧化二磷固体,所以可用来代替铜粉,故选A;
(2)液面至A装置的15cm刻度处后,A装置内气体的高度为15cm,其中氧气约占15cm×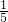 =3cm.因此反应完成后,A中液面应上升至15cm-3cm=12cm处.
=3cm.因此反应完成后,A中液面应上升至15cm-3cm=12cm处.
若液面升至13cm处,则15cm-13cm=2cm<3cm.说明实验结果比理论值偏小.
故答案为:(1)A;(2)12;偏小.
分析:(1)根据木炭和硫与氧气反应生成气体进行解答;
(2)根据空气中氧气的体积分数进行解答.
点评:本题主要考查空气中氧气含量方面的知识,解答时要注意测定氧气含量前,一定要检验装置的气密性.
(2)液面至A装置的15cm刻度处后,A装置内气体的高度为15cm,其中氧气约占15cm×
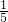 =3cm.因此反应完成后,A中液面应上升至15cm-3cm=12cm处.
=3cm.因此反应完成后,A中液面应上升至15cm-3cm=12cm处.若液面升至13cm处,则15cm-13cm=2cm<3cm.说明实验结果比理论值偏小.
故答案为:(1)A;(2)12;偏小.
分析:(1)根据木炭和硫与氧气反应生成气体进行解答;
(2)根据空气中氧气的体积分数进行解答.
点评:本题主要考查空气中氧气含量方面的知识,解答时要注意测定氧气含量前,一定要检验装置的气密性.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
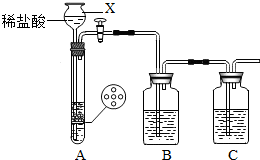 (2012?崇川区一模)某研究性学习小组设计并进行了如下实验.
(2012?崇川区一模)某研究性学习小组设计并进行了如下实验.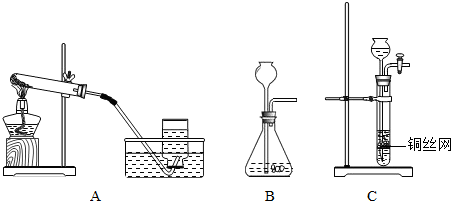
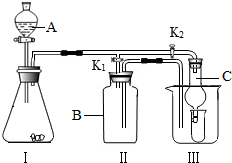 某研究性学习小组设计的实验装置(如图),既可制取气体,又可用于验证物质性质.
某研究性学习小组设计的实验装置(如图),既可制取气体,又可用于验证物质性质.