题目内容
26g黄铜(Cu-Zn合金)与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为125.8克.求:
(1)黄铜中铜的质量分数;
(2)所用稀硫酸中的溶质质量分数;
(3)反应后所得溶液中溶质质量分数.(计算结果精确到0.1%)
(1)黄铜中铜的质量分数;
(2)所用稀硫酸中的溶质质量分数;
(3)反应后所得溶液中溶质质量分数.(计算结果精确到0.1%)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:铜不能和稀硫酸反应,锌能和稀硫酸反应生成硫酸锌和氢气,反应前后的质量差即为生成氢气的质量;
根据氢气的质量可以计算锌的质量、反应的硫酸的质量和反应生成硫酸锌的质量,进一步可以计算黄铜中铜的质量分数、所用稀硫酸中的溶质质量分数、反应后所得溶液中溶质质量分数.
根据氢气的质量可以计算锌的质量、反应的硫酸的质量和反应生成硫酸锌的质量,进一步可以计算黄铜中铜的质量分数、所用稀硫酸中的溶质质量分数、反应后所得溶液中溶质质量分数.
解答:解:(1)设锌、硫酸、硫酸锌的质量分别为x、y、z,
生成氢气的质量为:26g+100g-125.8g=0.2g,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
x y z 0.2g
=
=
,
x=6.5g,y=9.8g,z=16.1g,
黄铜中铜的质量分数为:
×100%=75%,
答:黄铜中铜的质量分数为75%.
(2)所用稀硫酸中的溶质质量分数为:
×100%=9.8%,
答:所用稀硫酸中的溶质质量分数为9.8%.
(3)反应后所得溶液中溶质质量分数为:
×100%=15.1%,
答:反应后所得溶液中溶质质量分数为15.1%.
生成氢气的质量为:26g+100g-125.8g=0.2g,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
x y z 0.2g
| 65 |
| x |
| 98 |
| y |
| 161 |
| z |
| 2 |
| 0.2g |
x=6.5g,y=9.8g,z=16.1g,
黄铜中铜的质量分数为:
| 26g-6.5g |
| 26g |
答:黄铜中铜的质量分数为75%.
(2)所用稀硫酸中的溶质质量分数为:
| 9.8g |
| 100g |
答:所用稀硫酸中的溶质质量分数为9.8%.
(3)反应后所得溶液中溶质质量分数为:
| 16.1g |
| 6.5g+100g-0.2g |
答:反应后所得溶液中溶质质量分数为15.1%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
下列关于化学与生活、科技的描述中无科学性错误的是( )
| A、食盐可用作食品防腐剂 |
| B、河水“富营养化”有利于动植物的生长 |
| C、糖尿病人可多吃大米等无甜味的食物 |
| D、雾霾天气是雨后空气湿度大造成的 |
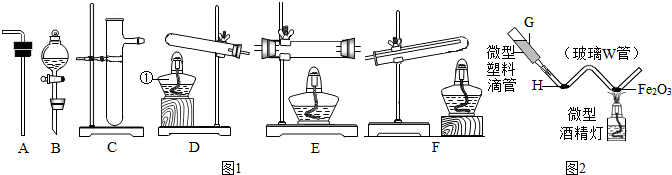
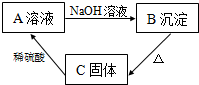 材料:难溶于水的碱在加热的条件下,容易分解生成对应的金属氧化物和水.
材料:难溶于水的碱在加热的条件下,容易分解生成对应的金属氧化物和水.